题目内容
能正确表示下列反应的离子方程式是( )
| A、向漂白液中通入过量CO2:ClO-+H2O+CO2═HClO+HCO3- |
| B、将磁性氧化铁溶于盐酸:Fe3O4+8H+═3Fe3++4H2O |
| C、氯气与水反应:Cl2+H2O═2H++Cl-+ClO- |
| D、将铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.二氧化碳过量,碳酸钙沉淀溶解,反应生成次氯酸和碳酸氢根离子;
B.该离子方程式两边电荷不守恒,四氧化三铁与盐酸反应生成铁离子和亚铁离子;
C.次氯酸为弱电解质,离子方程式中次氯酸不能拆开;
D.铁与稀盐酸反应生成亚铁离子和氢气,不会生成铁离子.
B.该离子方程式两边电荷不守恒,四氧化三铁与盐酸反应生成铁离子和亚铁离子;
C.次氯酸为弱电解质,离子方程式中次氯酸不能拆开;
D.铁与稀盐酸反应生成亚铁离子和氢气,不会生成铁离子.
解答:
解:A.向漂白液中通入过量CO2,反应生成次氯酸和碳酸氢根离子,反应的离子方程式为:ClO-+H2O+CO2═HClO+HCO3-,故A正确;
B.将磁性氧化铁溶于盐酸,反应生成亚铁离子、铁离子,正确的离子方程式为:Fe3O4+8H+═Fe2++2Fe3++4H2O,故B错误;
C.氯气与水反应生成氯化氢和次氯酸,次氯酸应该保留分子式,正确的离子方程式为:Cl2+H2O═H++Cl-+HClO,故C错误;
D.铁粉加入稀硫酸中,反应生成铁离子和氢气,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故D错误;
故选A.
B.将磁性氧化铁溶于盐酸,反应生成亚铁离子、铁离子,正确的离子方程式为:Fe3O4+8H+═Fe2++2Fe3++4H2O,故B错误;
C.氯气与水反应生成氯化氢和次氯酸,次氯酸应该保留分子式,正确的离子方程式为:Cl2+H2O═H++Cl-+HClO,故C错误;
D.铁粉加入稀硫酸中,反应生成铁离子和氢气,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故D错误;
故选A.
点评:本题考查了离子方程式的书写判断,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
相关题目
除去下列溶液中的杂质(括号内是杂质)所用试剂不正确的是( )
| A、Fe(Al):用NaOH溶液 |
| B、NaCl溶液(Na2CO3):用盐酸 |
| C、K2SO4溶液(K2CO3):用H2SO4溶液 |
| D、NaCl溶液 (HCl):用AgNO3溶液 |
下列说法不正确的是( )
| A、加入苯酚显紫色的溶液:K+、NH4+、Cl-、I-;加入酚酞呈红色的溶液:SO42-、K+、Cl-、HSO3- 分别都不能大量共存(常温下) | ||
B、
| ||
| C、已知:25℃时,Mg(OH)2的kSP=5.61×10-12,MgF2的kSP=7.42×10-11,25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2 可以转化为MgF2 | ||
D、表示H2燃烧热的化学方程式为:H2(g)+
|
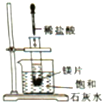 如图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.下列说法不正确的是( )
如图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.下列说法不正确的是( )| A、试管中有气泡产生 |
| B、烧杯内出现浑浊 |
| C、镁条的化学能大于氢气 |
| D、镁条与稀盐酸的反应为放热反应 |
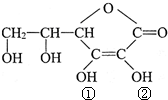 维生素C(VitaminC)又名抗坏血酸,具有酸性和强还原性,也是一种常见的食品添加剂,结构如图,下列关于维生素C正确的是( )
维生素C(VitaminC)又名抗坏血酸,具有酸性和强还原性,也是一种常见的食品添加剂,结构如图,下列关于维生素C正确的是( )| A、维生素C能使酸性高锰酸钾溶液褪色 |
| B、维生素C由于含有酯基而难溶于水 |
| C、维生素C酸性可能是①②两个羟基引起的 |
| D、维生素C由于含有C=O键而能发生银镜反应 |
在组装原电池时,下列各项中不需要的是( )
| A、电极材料 | B、直流电源 |
| C、电解质溶液 | D、金属导线 |
化学工业是国民经济的支柱产业,下列生产过程中不涉及氧化还原反应的是( )
| A、纯碱厂用侯氏制碱法制纯碱 |
| B、硝酸厂用氨氧化法制硝酸 |
| C、硫酸厂用接触法生产硫酸 |
| D、氮肥厂用氮气和氢气合成氨气 |
 2003年10月16日“神舟五号”飞船成功发射,实现了中华民族的飞天梦想.运送飞船的火箭燃料除液态双氧水外,还有另一种液态氮氢化合物.已知该化合物中氢元素的质量分数为12.5%,相对分子质量为32,结构分析发现该分子结构中只有单键.
2003年10月16日“神舟五号”飞船成功发射,实现了中华民族的飞天梦想.运送飞船的火箭燃料除液态双氧水外,还有另一种液态氮氢化合物.已知该化合物中氢元素的质量分数为12.5%,相对分子质量为32,结构分析发现该分子结构中只有单键.
 与
与 