题目内容
19.下列选项中两物质所含原子数目一定相等的是( )| A. | 相同体积,不同密度的N2和CO两种气体 | |
| B. | 相同密度的O2和O3两种气体 | |
| C. | 相同质量,不同密度的C2H4和C3H8两种气体 | |
| D. | 相同物质的量,不同体积的NH3和CH4两种气体 |
分析 A、体积相同、密度不同,则质量不同,根据N=nNA=NA结合分子构成判断;
B、两气体的体积大小是否相等不明确;
C、C2H4和C3H8的最简式均为CH2;
D、1mol氨气中含4mol原子,1mol甲烷中含5mol原子.
解答 解:A、体积相同、密度不同,则质量不同,由N=nNA=NA知,两种气体的质量不相同,但摩尔质量相同,所以所含分子数不相同,且氮气和一氧化碳都是双原子分子,所以含有的原子数不相同,故A错误;
B、两气体的体积大小是否相等不明确,则质量是否相等不明确,故含有的氧原子的个数是否相等不明确,故B错误;
C、C2H4和C3H8的最简式均为CH2,故相同质量的量气体中含有的CH2的物质的量均相等,则含由的原子的物质的量均相等,故C正确;
D、1mol氨气中含4mol原子,1mol甲烷中含5mol原子,故等物质的量的两气体中的原子的物质的量之比为4:5,故D错误.
故选C.
点评 本题考查原子数的有关计算,以及阿伏加德罗定律及推论,题目难度不大,注意把握物质的量、质量、体积之间的计算公式的运用.

练习册系列答案
相关题目
7.设NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1 mol NaHSO4晶体中离子总数为3NA | |
| B. | 2.24L14CH4分子中所含中子数为0.8NA | |
| C. | 0.1L 3 mol•L-1的NH4NO3溶液中含有的NH4+数目为0.3 NA | |
| D. | 标况下,将FeSO4溶液置于空气中,被氧化的Fe2+为0.2 NA,吸收O2为1.12 L |
14.为了延长食品的保质期,防止食品受潮及富脂食品氧化变质,在包装袋中可装入的物质是( )
| A. | 无水硫酸铜、蔗糖 | B. | 硅胶、硫酸亚铁 | C. | 食盐、硫酸亚铁 | D. | 生石灰、食盐 |
4.有8gNa2O2、Na2O、Na2CO3、NaOH的混合物与200g质量分数为3.65%的盐酸恰好完全反应,蒸干溶液,最终得到的固体质量为( )
| A. | 8g | B. | 15.5g | C. | 11.7g | D. | 无法确定 |
11. 某无色溶液,可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现各取两份100mL溶液进行如下实验:
某无色溶液,可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现各取两份100mL溶液进行如下实验:
①第一份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为9.32g.
②第二份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图.
已知:2Al3++2CO32-+3H2O=2Al(OH)3↓+3CO2↑
(1)由此推断,原溶液一定含有的阳离子种类及其浓度,将结果填入下表(可不填满).
(2)无法确定的离子是NO3-,如何通过进一步实验确证未确定的离子是否存在?用小试管取少量溶液,加入少量浓硫酸,再向试管中加入铜屑并加热,产生的气体在空气中变成红棕色证明含有硝酸根离子..
 某无色溶液,可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现各取两份100mL溶液进行如下实验:
某无色溶液,可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现各取两份100mL溶液进行如下实验:①第一份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为9.32g.
②第二份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图.
已知:2Al3++2CO32-+3H2O=2Al(OH)3↓+3CO2↑
(1)由此推断,原溶液一定含有的阳离子种类及其浓度,将结果填入下表(可不填满).
| 一定含有的阳离子种类 | ||||||
| 物质的量浓度(mol/L) |
17.某化学小组通过查阅资料,设计了如图所示的方法以含镍废催化剂为原料来制备NiSO4•7H2O.已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%).

部分阳离子以氢氧化物形式沉淀时的pH如表:
(1)操作a、c中需使用的仪器除铁架台(带铁圈)、酒精灯、烧杯、玻璃棒外,还需要的主要仪器有漏斗、蒸发皿.
(2)“碱浸”过程中发生反应的离子方程式有Al2O3+2OH-═2AlO+H2O、2Al+2OH-+2H2O═2AlO2-+3H2↑.
(3)“酸浸”时所加入的酸是H2SO4(填化学式).
(4)操作b为调节溶液的pH,你认为pH的调控范围是3.2-7.1.
(5)产品晶体中有时会混有少量绿矾(FeSO4•7H2O),其原因可能是H2O2的用量不足(或H2O2失效)、保温时间不足导致Fe2+未被完全氧化造成的(写出一点即可).

部分阳离子以氢氧化物形式沉淀时的pH如表:
| 沉淀物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| Fe(OH)2 | 7.6 | 9.7 |
| Ai(OH)2 | 7.1 | 9.2 |
(2)“碱浸”过程中发生反应的离子方程式有Al2O3+2OH-═2AlO+H2O、2Al+2OH-+2H2O═2AlO2-+3H2↑.
(3)“酸浸”时所加入的酸是H2SO4(填化学式).
(4)操作b为调节溶液的pH,你认为pH的调控范围是3.2-7.1.
(5)产品晶体中有时会混有少量绿矾(FeSO4•7H2O),其原因可能是H2O2的用量不足(或H2O2失效)、保温时间不足导致Fe2+未被完全氧化造成的(写出一点即可).

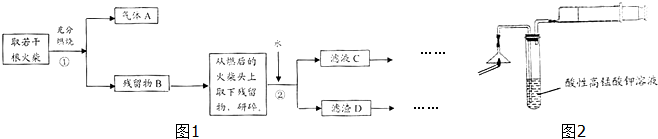


 .
. 结构且能水解的所有同分异构体的结构简式:
结构且能水解的所有同分异构体的结构简式: .
.
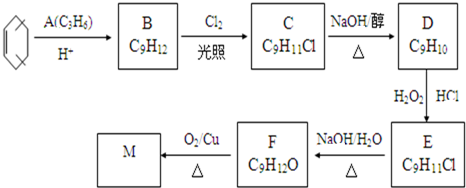
 ;
; ;
;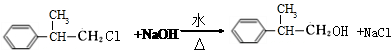 .
.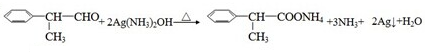 .
.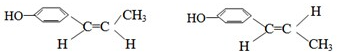 .
.