题目内容
3.某混合气体由两种气态烃组.标准状况下,2.24L 该混合气体完全燃烧后,得到3.36L二氧化碳气体(标准状况)和3.6g水.下列说法中正确的是( )| A. | 混合气体中一定含有甲烷 | B. | 混合气体一定是甲烷和乙烯 | ||
| C. | 混合气体中一定含有乙烷 | D. | 混合气体可能是甲烷和乙烯 |
分析 根据n=$\frac{m}{M}$计算3.6g水的物质的量,根据n=$\frac{V}{{V}_{m}}$计算出混合烃、二氧化碳的物质的量,根据H原子、C原子守恒计算混合物的平均分子组成,然后对各选项进行判断.
解答 解:标准状况下2.24L混合烃的物质的量为:n=$\frac{2.24L}{22.4L/mol}$=0.1mol,
3.6g水的物质的量为:n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,平均分子式中含有的H原子数目为:$\frac{0.2mol×2}{0.1mol}$=4,
3.36L二氧化碳的物质的量为:n=$\frac{3.36L}{22.4L/mol}$=0.15mol,平均分子式中含有的C原子数目为:$\frac{0.15mol}{0.1mol}$=1.5,
则该混合烃的平均分子式为:C1.5H4,
根据C原子可知,烃中碳原子数小于1的只有甲烷,则该烃中一定含有CH4;
甲烷分子中含有4个H原子,而平均分子式中H原子数为4,则另一烃的分子中H原子数目为4,
A.根据分析可知,混合气体中一定含有甲烷,故A正确;
B.混合气体中一定含有甲烷,可能含有乙烯,故B错误;
C.乙烷分子中含有6个H,不满足条件,故C错误;
D.混合气体中可能含有甲烷和乙烯,故D正确;
故选AD.
点评 本题考查有机物分子的判断,题目难度中等,解题关键是掌握利用平均分子组成判断烃的组成的方法,试题充分培养了学生的分析能力及化学计算能力.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
14.用53g Na2CO3固体配成2L溶液,则Na2CO3的物质的量浓度为( )
| A. | 0.25mol•L-1 | B. | 0.50mol•L-1 | C. | 0.75mol•L-1 | D. | 1.25mol•L-1 |
11.有Al、CuO、Fe2O3组成的混合物共10.0g,放入250mL某浓度的硫酸溶液中,混合物完全溶解,当再加入125mL 2.00mol/L的NaOH溶液时,得到沉淀物质的量最多.上述硫酸溶液的浓度为( )
| A. | 0.500 mol/L | B. | 1.00 mol/L | C. | 2.00 mol/L | D. | 3.00 mol/L |
15.镍镉电池是一种可充电电池,该电池放电时的总反应为:Cd+2NiOOH+2H2O=Cd(OH)2+2Ni(OH)2 下列说法错误的是( )
| A. | 该电池的电解液可以选用KOH溶液,负极是Cd,正极是NiOOH | |
| B. | 该电池放电时,负极反应为:Cd-2e-+2OH-=Cd(OH)2 | |
| C. | 该电池充电过程中,阴极附近的溶液PH降低 | |
| D. | 该电池充电时,阳极反应为:2Ni(OH)2-2e-+2OH-=2NiOOH+2H2O |
 氢能被视作连接化石能源和可再生能源的重要桥梁.
氢能被视作连接化石能源和可再生能源的重要桥梁.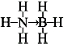 ;与氨硼烷互为等电子体的有机化合物是CH3CH3(写结构简式).
;与氨硼烷互为等电子体的有机化合物是CH3CH3(写结构简式).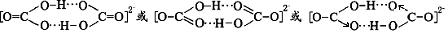 .
.