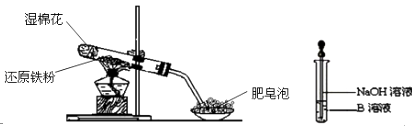
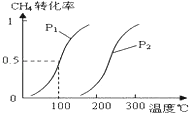
��Ŀ����
����Ŀ��A��B��C��D��Ԫ�����ڱ��еĶ�����Ԫ�أ���ԭ��������������AԪ��ԭ���������ӣ�BԪ�ص�һ��ͬλ�س���������ţ��Ҹ�Ԫ���γɵĻ�����������࣬DԪ�ص�ԭ�Ӻ��������������Ǵ������������������ش��������⣺
��1��DԪ�صķ����� �� CԪ����ɵĵ���C2�ĵ���ʽ�� ��
��2��2016��10��17��7��30���ڸ���ľ�Ȫ���Ƿ�����أ��ҹ��ɹ����䡰����ʮһ�š����˷ɴ�������ķ�����ȼ�ϸ���ΪҺ̬ƫ�����£�����ʽΪC2H8N2����������ΪҺ̬��C2D4 �� ȼ�պ����Ի�������Ⱦ��д��ƫ��������C2D4��Ӧ�Ļ�ѧ����ʽ��
��3��C2A4����Ϊ�����������ȼ�ϣ���������C2D4��Ӧ����C2��A2D����֪��
��C2��g��+2D2��g���TC2D4��L����H1�T��19.5kJ/mol
��C2A4��L��+D2��g���TC2��g��+2A2D��g����H2�T��534.2kJ/mol
д��Һ��ȼ��C2A4��Һ̬C2D4��Ӧ���Ȼ�ѧ����ʽ�� ��
��4����230��ʹ������ڵ������£���BD2��A2ת��ΪBA3DA��g����A2D��g������ͼΪ����1mol BA3DA��g���������仯ʾ��ͼ�� 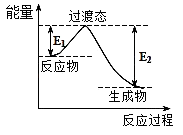
��֪�ƻ�1mol��ͬ���ۼ���������kJ���ֱ��ǣ�
B��A | B��D | B=D | A��A | A��D |
413.4 | 351 | 745 | 436 | 462.8 |
��д��BD2��A2ת��Ϊ1mol BA3DA��g����A2D��g�����Ȼ�ѧ����ʽ��
����֪E1=8.2kJmol��1 �� ��E2=kJmol��1 ��
���𰸡�
��1��O��![]()
��2��C2H8N2+2N2O4=3N2+4H2O+2CO2
��3��2N2H4��L��+N2O4��l��=3N2��g��+4H2O��g����H=��1048.9kJ/mol
��4��CO2��g��+3H2��g��=CH3OH��g��+H2O��g����H�T��181.6kJ/mol��189.8
���������⣺A��B��C��D��Ԫ�����ڱ��еĶ�����Ԫ�أ���ԭ��������������AԪ��ԭ���������ӣ���AΪHԪ�أ�BԪ�ص�һ��ͬλ�س���������ţ��Ҹ�Ԫ���γɵĻ�����������࣬��BΪCԪ�أ�
DԪ�ص�ԭ�Ӻ��������������Ǵ�����������������ΪOԪ�أ���CΪNԪ�أ���1��D��OԪ�أ�CԪ����ɵĵ���N2 �� ���������е�ԭ��֮�乲��3�Ե�����ÿ��Nԭ�Ӻ���һ���µ��Ӷԣ�����ʽΪ ![]() �����Դ��ǣ�O��
�����Դ��ǣ�O�� ![]() ����2��C2H8N2��������N2O4���ȼ�պ����Ի�������Ⱦ��˵�����ɵ�����������̼��ˮ����Ӧ����ʽΪC2H8N2+2N2O4=3N2+4H2O+2CO2 �� ���Դ��ǣ�C2H8N2+2N2O4=3N2+4H2O+2CO2����3��N2H4��������N2O4��Ӧ����N2��H2O����N2��g��+2O2��g���TN2O4��l����H1�T��19.5kJ/mol��N2H4��l��+O2��g���TN2��g��+2H2O��g����H2�T��534.2kJ/mol
����2��C2H8N2��������N2O4���ȼ�պ����Ի�������Ⱦ��˵�����ɵ�����������̼��ˮ����Ӧ����ʽΪC2H8N2+2N2O4=3N2+4H2O+2CO2 �� ���Դ��ǣ�C2H8N2+2N2O4=3N2+4H2O+2CO2����3��N2H4��������N2O4��Ӧ����N2��H2O����N2��g��+2O2��g���TN2O4��l����H1�T��19.5kJ/mol��N2H4��l��+O2��g���TN2��g��+2H2O��g����H2�T��534.2kJ/mol
������ʽ2�ک��ٵ�2N2H4 ��l��+N2O4 ��l��=3N2 ��g��+4H2O ��g����H�T2������534.2kJ/mol��������19.5kJ/mol��=��1048.9kJ/mol��
���Դ��ǣ�2N2H4 ��l��+N2O4 ��l��=3N2 ��g��+4H2O ��g����H=��1048.9kJ/mol����4������230��ʹ������ڵ������£���CO2��H2ת��ΪCH3OH��g����H2O��g����
�÷�Ӧ����ʽΪCO2 ��g��+3H2 ��g��=CH3OH��g��+H2O��g����H=��745��2+3��436��413.4��3��351��462.8��462.8��2��kJ/mol=��181.6kJ/mol��
���Դ��ǣ�CO2 ��g��+3H2 ��g��=CH3OH��g��+H2O��g����H�T��181.6kJ/mol��
�ڸ���ͼ֪���÷�Ӧ�Ƿ��ȷ�Ӧ��E1=8.2kJmol��1 �� ��H=����E2��E1��=��181.6kJ/mol������E1=8.2kJmol��1 �� E2=189.8kJmol��1 ��
���Դ��ǣ�189.8��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ����������4�����ʣ� A��NaOH��Ca��OH��2��SO2��Fe��OH��3
B��Cl2��C��S��Cu
C��Hg��Cu��Zn��H2
D��H2O��HCl��H2SO4��HNO3
��1����д���пհף�
A�� | B�� | C�� | D�� | |
����� | ���������� | |||
�����ڸ��������� | SO2 | H2 | H2O |
��2��4�������ж����ڵ���ʵ���������ţ���
��3��д��ʵ�����Ʊ�Cl2�����ӷ���ʽΪ ��