题目内容
瑞典ASES公司设计的用于驱动潜艇的液氨-液氧燃料 电池示意图如下,有关说法正确的是
| A.电池总反应为:4NH3 + 3O2 = N2 + 6H2O |
| B.电池工作时,OH-向负极移动 |
| C.电极2发生的电极反应为:O2+4H+ + 4e-=2H2O |
| D.电流由电极1经外电路流向电极2 |
B
解析试题分析:A、该化学方程式没有配平,错误;B、电池工作时,阴离子向负极移动,正确;C、该电池的电解质溶液为NaOH溶液,所以电极2发生的电极反应为:O2+2H2O+4e?=4OH?,错误;D、电流由正极流向负极,所以电流由电极2经外电路流向电极1,错误。
考点:本题考查原电池原理。

练习册系列答案
 优等生题库系列答案
优等生题库系列答案
相关题目
如图是用氢氧燃料电池电解氯化钠溶液(均为惰性电极),下列说法正确的是 ( )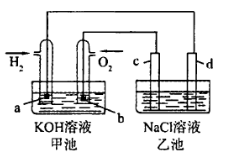
| | 甲池 | 乙池 |
| A | 放电过程中氢氧化钾浓度不变 | 滴加酚酞试液d区域溶液先变红 |
| B | 氢氧根向a极移动 | 氢氧根移向d极 |
| C | a电极消耗2.24L氢气时 | c电极生成1.12L氧气 |
| D | a电极反应:H2 -2e- =2H+ | d电极反应:4OH- -4e-=O2 + 2H2O |
电解硫酸溶液时,放出25mL(标况)O2,若以等量的电量在同样条件下电解盐酸溶液,
所放出的气体的体积最接近下列数据中的
| A.45mL | B.50mL | C.75mL | D.100mL |
某原电池总反应为:Cu+2Fe3+=Cu2++2Fe2+下列能实现该反应的原电池是
| | A | B | C | D |
| 电极材料 | Cu、Zn | Cu、Ag | Cu、C | Fe、Zn |
| 电解液 | FeCl3 | Fe2(SO4)3 | Fe(NO3)2 | CuSO4 |
一种充电电池放电时的电极反应为:H2+2OH--2e-=2H2O NiO(OH)+H2O+e-=Ni(OH)2+OH-
当为电池充电时,与外电源正极连接的电极上发生的反应是( )
| A.H2O的还原 | B.NiO(OH)的还原 |
| C.H2的氧化 | D.Ni(OH)2的氧化 |
某新型碱性可充电电池,能长时间保持稳定的放电电压。该电池的总反应为3Zn+2K2FeO4+8H2O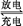 3Zn(OH)2+2Fe(OH)3+4KOH,以下说法错误的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,以下说法错误的是( )
| A.电池放电是化学能转化成电能的过程 |
B.放电时正极反应为:Fe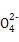 +4H2O+3e- +4H2O+3e-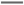 Fe(OH)3+5OH- Fe(OH)3+5OH- |
| C.充电时电池的负极接外电源的正极 |
| D.充电时电解质溶液中的阴离子向阳极定向移动 |
用惰性电极电解一定量的硫酸铜溶液,实验装置如下图甲。电解过程中的实验数据如下图乙,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况)。则下列说法不正确的是( )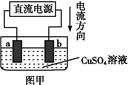
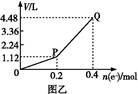
| A.电解过程中,a电极表面先有红色物质析出,后有气泡产生 |
B.b电极上发生的反应方程式为:4OH--4e- 2H2O+O2↑ 2H2O+O2↑ |
| C.曲线0~P段表示O2的体积变化 |
| D.从开始到Q点时收集到的混合气体的平均摩尔质量为12 g/mol |
关于铅蓄电池的说法正确的是( )。
| A.在放电时,正极发生的反应是Pb(s)+SO42-(aq)-2e-=PbSO4(s) |
| B.在放电时,该电池的负极材料是铅板 |
| C.在充电时,电池中硫酸的浓度不断变小 |
| D.在充电时,阳极发生的反应是PbSO4(s)+2e-=Pb(s)+SO42-(aq) |
下列叙述中不正确的是( )
| A.电解池的阳极上发生氧化反应,阴极上发生还原反应 |
| B.原电池的正极上发生氧化反应,负极上发生还原反应 |
| C.电镀时,电镀池里的阳极材料发生氧化反应 |
| D.用原电池做电源进行电解时,电子从原电池负极流向电解池阴极 |