题目内容
电解硫酸溶液时,放出25mL(标况)O2,若以等量的电量在同样条件下电解盐酸溶液,
所放出的气体的体积最接近下列数据中的
| A.45mL | B.50mL | C.75mL | D.100mL |
D
解析试题解析:每生成1mol的氧气则转移4mol电子,而相同的电量电解盐酸产生的氯气、氢气各得2mol,共4mol,所以以等量的电量在同样条件下电解盐酸产生的气体体积是氧气体积的4倍,故该体积应为100ml,答案选D。
考点:考查电解原理及相应计算

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
瑞典ASES公司设计的用于驱动潜艇的液氨-液氧燃料 电池示意图如下,有关说法正确的是
| A.电池总反应为:4NH3 + 3O2 = N2 + 6H2O |
| B.电池工作时,OH-向负极移动 |
| C.电极2发生的电极反应为:O2+4H+ + 4e-=2H2O |
| D.电流由电极1经外电路流向电极2 |
在电解水制取H2和O2时,为了增强导电性常常要加入一些电解质,最好选用
| A.NaOH | B.HCl | C.NaCl | D.CuSO4 |
如图所示,a、b、c均为石墨电极,d为碳钢电极,通电电解一段时间。假设在电解过程中产生的气体全部逸出,下列说法正确的是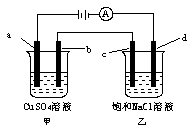
| A.甲、乙两烧杯中溶液的pH均保持不变 |
| B.甲烧杯中a电极反应式为:4OH――4e-=O2↑+2H2O |
| C.当电解一段时间后,将甲、乙两溶液混合,一定会产生蓝色沉淀 |
| D.当b极增重3.2 g时,d极产生的气体为0.56 L(标准状况) |
已知X、Y在一定条件下发生反应,可以得到E、F、G。下列假设与结论能对应成立的是( )
| 选项 | 假设 | 结论 |
| A | 若X、Y均为固体,E为气体 | 则E一定能使湿润的蓝色石蕊试纸变红 |
| B | 若该反应是氯碱工业的主要反应,反应一段时间后 | 两极产生的气体体积可能不同(不考虑气体的溶解) |
| C | 若X为单质,Y为氧化性酸,气体E是能引起酸雨的主要物质 | 则Y一定是浓H2SO4 |
| D | 若X为有机物,得到E是一种红色沉淀 | 则X一定是醛 |
燃料电池能有效提高能源利用率,具有广泛的应用前景。下列物质均可用作燃料电池的燃料,其中最环保的是( )
| A.甲醇 | B.天然气 | C.液化石油气 | D.氢气 |
如图,a、b是石墨电极,通电一段时间后,b极附近溶液显红色。下列说法正确的是( ) 
| A.X极是电源负极,Y极是电源正极 |
| B.a极的电极反应是2Cl--2e-=Cl2↑ |
| C.电解过程中CuSO4溶液的pH逐渐增大 |
| D.Pt极上有6.4 g Cu析出时,b极产生2.24 L(标准状况)气体 |
电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。
已知:3I2+6OH-=IO3—+5I-+3H2O
下列说法不正确的是 ( )。
| A.右侧发生的电极反应式:2H2O+2e-=H2↑+2OH- |
| B.电解结束时,右侧溶液中含IO3— |
C.电解槽内发生反应的总化学方程式:KI+3H2O KIO3+3H2↑ KIO3+3H2↑ |
| D.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学反应不变 |
如图,A池用石墨电极电解NaOH溶液,B池精炼粗铜,一段时间后停止通电,A池中d极产生具有氧化性的气体,在标准状况下为2.24 L。下列说法正确的是( )
| A.A池为电解池,B池为原电池 |
| B.d、e两极都发生氧化反应 |
| C.e极应为粗铜板材料 |
| D.B池中e极质量增加12.8 g |