题目内容
13.设NA代表阿伏加德罗常数,下列叙述正确的是( )| A. | 20℃时,1mol SO2的体积一定大于22.4L | |
| B. | 常温常压下,1mol CO2与18 g H2O所含有的原子总数均为3 NA | |
| C. | 1mol/LNaCl溶液表示1L水中含有NaCl 58.5g | |
| D. | 标准状况下,11.2L NO与5.6 L O2形成的混合气体中含有的分子数为0.5NA |
分析 A、压强不明确;
B、18g水的物质的量为1mol,而 CO2与 H2O均为3原子分子;
C、1mol/LNaCl溶液表示1L溶液中含有氯化钠2mol;
D、一氧化氮与氧气混合会发生反应生成二氧化氮,所以混合后气体的物质的量减小,分子数目减小.
解答 解:A、压强不明确,故气体摩尔体积的数值不明确,则1mol二氧化硫的体积不能计算,故A错误;
B、18g水的物质的量为1mol,而 CO2与 H2O均为3原子分子,故1mol二氧化碳和水中均含3mol原子即3NA个,故B正确;
C、1mol/LNaCl溶液表示1L溶液中含有氯化钠1mol,即58.5g,故C错误;
D、标准状况下,11.2L气体的物质的量为0.5mol,0.5mol一氧化氮与0.25mol氧气混合,生成的0.5mol二氧化氮中存在平衡:2NO2?N2O4,所以混合后的气体物质的量小于0.5mol,所含分子数小于0.5NA,故D错误,.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
4.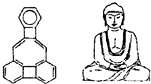 美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛.有关该有机分子的说法正确的是( )
美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛.有关该有机分子的说法正确的是( )
 美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛.有关该有机分子的说法正确的是( )
美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛.有关该有机分子的说法正确的是( )| A. | 该有机物属于芳香烃 | B. | 该有机物属于苯的同系物 | ||
| C. | 该有机物分子中含有23个碳原子 | D. | 该有机物的一氯代物有3种 |
1.北京奥运会的“祥云”火炬所用燃料的主要成分是丙烷,下列有关丙烷的叙述中不正确的是( )
| A. | 分子中碳-碳原子间是非极性共价键 | |
| B. | 光照下能够发生取代反应 | |
| C. | 比丁烷更易液化 | |
| D. | 是石油分馏的一种产物 |
18.某物质结构简式如右图所示,下列有关该物质的说法不正确的是( )


| A. | 该物质分子式为C13H14O4 | |
| B. | 能与FeCl3溶液发生显色反应 | |
| C. | 在一定条件下可发生加成、取代、消去反应 | |
| D. | 1 mol该物质最多能与2mol NaOH反应 |
5.下列离子方程式与所述事实相符且正确的是( )
| A. | 用食醋和淀粉-KI试纸检验碘盐中的KIO3:IO3-+5I-+6H+═3I2+3H2O | |
| B. | 稀HNO3溶液与难溶于水的FeS固体:FeS+2H+═Fe2++H2S↑ | |
| C. | 碳酸氢钙与少量的NaOH溶液反应 Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| D. | Na与水的反应Na+H2O═Na++OH-+H2↑ |
2.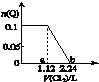 向含Fe2+、Br-、I-各0.1mol的溶液中通入标准状况下的Cl2,通入Cl2的体积和溶液中某种离子的物质的量的关系如图,下列说法中正确的是( )
向含Fe2+、Br-、I-各0.1mol的溶液中通入标准状况下的Cl2,通入Cl2的体积和溶液中某种离子的物质的量的关系如图,下列说法中正确的是( )
 向含Fe2+、Br-、I-各0.1mol的溶液中通入标准状况下的Cl2,通入Cl2的体积和溶液中某种离子的物质的量的关系如图,下列说法中正确的是( )
向含Fe2+、Br-、I-各0.1mol的溶液中通入标准状况下的Cl2,通入Cl2的体积和溶液中某种离子的物质的量的关系如图,下列说法中正确的是( )| A. | Q是I- | |
| B. | Q是Br- | |
| C. | ab区间的反应:2Fe2++Cl2═2Fe3++2Cl- | |
| D. | b点时溶液中只有Cl- |
3.已知10.2g A与12.8g B完全反应,生成9.6g C和7.2g D及另一气体E,已知E的密度是H2密度的15.5倍.则气体E在标准状况下的体积( )
| A. | 2.24L | B. | 4.48L | C. | 5.6L | D. | 11.2L |
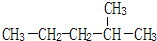 2-甲基戊烷
2-甲基戊烷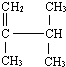 2,3-二甲基-1-丁烯
2,3-二甲基-1-丁烯 1,2-二溴乙烷
1,2-二溴乙烷 乙苯
乙苯