题目内容
(8分,每空1分)
(1)玻璃棒、100mL容量瓶 (只答“容量瓶”0分)
(2)28.6
(3)刻度线(标线)、温度、容量(体积)
(4)直接倒入容量瓶中,没有用玻璃棒引流,定容后没有将容量瓶倒转摇匀(每答对一处得1分)
解析试题分析:实验室用碳酸钠晶体配制1.00 mol/L的溶液l00mL,(1)所需主要仪器为:药匙、托盘天平、烧杯、量筒、玻璃棒、100mL容量瓶和胶头滴管;
(2)本实验须称量碳酸钠晶体(Na2CO3.10H2O)为1.00 mol/L×0.1L×286g/mol=28.6g。
(3)容量瓶上标有刻度线(标线)、温度25℃、容量(体积)100mL。
(4)某同学将称量好的碳酸钠晶体用适量的蒸馏水在烧杯中溶解,冷却后直接倒进(应用玻璃棒引流)所选的且经检查不漏水的容量瓶中,洗涤烧杯2—3次,洗涤液也移至容量瓶中,晃动容量瓶使其混合均匀,然后加水至离刻度线2cm处,用胶头滴管加水至刻度线(然后摇混合均匀),倒入试剂瓶贴上标签备用。
考点:实验室用碳酸钠晶体配制1.00 mol/L的溶液l00mL的实验及评价。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.常温下,18g H2O中含H2数目为NA |
| B.标准状况下,22. 4LH2O中含有化学键的数目为2NA |
| C.将0.5mol SO2通入足量水中,充分反应后可得到H2 SO3分子数为0.5NA |
| D.常温常压下,Na2O2与足量H2O反应,共生成0.2mol O2,转移电子的数目为0.4 NA |
下列各项中表达不正确的是
A.F-的结构示意图: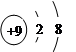 |
B.NaCl的电子式: |
| C.CO2的分子结构式: O=C=O |
| D.碳-12原子 |
(8分)某同学按下列步骤配制500 mL 0.2 mol·L-1 KCl溶液,请回答有关问题。
| 实验步骤 | 有关问题 |
| ①计算所需KCl的质量 | 需要KCl的质量为________g(保留小数点后一位) |
| ②称量KCl固体 | 称量需要用到的主要仪器是________________ |
| ③将KCl加入100 mL烧杯中,并加入适量水 | 为了加快溶解速率,可以采取哪些措施? ________________ |
| ④将烧杯中溶液转移至500 mL容量瓶中 | 为了防止溶液溅出,应采取什么措施? __________________ |
| ⑤向容量瓶中加蒸馏水至刻度线 | 在进行此操作时当加水至离刻度线1 cm~2 cm处应如何操作?____________________ |
(2)在进行④步操作时未将洗涤烧杯、玻璃棒的洗涤液转移至容量瓶,则配制溶液浓度
________(填“偏高”、“偏低”或“不影响”)。
(3)若进行⑤步操作时加蒸馏水超过刻度线,则需________。