题目内容
【题目】下列说法不正确的是( )
A. 光催化还原水制氢比电解水制氢更节能环保、更经济
B. 氨氮废水(含NH4+及NH3)可用化学氧化法或电化学氧化法处理
C. 某种光学检测技术具有极高的灵敏度,可检测到单个细胞(V≈10-12L)内的数个目标分子,据此可推算该检测技术能测量细胞内浓度约为10-12~10-11mol·L-1的目标分子
D. 向汽油中添加甲醇后,该混合燃料的热值不变
【答案】D
【解析】A.光催化更环保经济,电解需耗费大量能源,故A正确;B、氨氮废水中N为-3价,可利用氧化还原反应原理发生氧化反应转化为无毒物质,所以可用化学氧化法或电化学氧化法处理,故B正确;C、可检测到单个细胞(V≈10-12L)内的数个目标分子,体积为10-12L,设数个分子为N,则即该检测技术能检测细胞内浓度为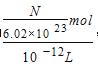 ,N可能介于1~10之间,则约为10-12-10-11molL-1的目标分子,故C正确;D、汽油和甲醇的热值不同,所以向汽油中添加甲醇后,该混合燃料的热值会改变,故D错误;故选D。
,N可能介于1~10之间,则约为10-12-10-11molL-1的目标分子,故C正确;D、汽油和甲醇的热值不同,所以向汽油中添加甲醇后,该混合燃料的热值会改变,故D错误;故选D。

【题目】XYZWR是前三周期常见元素,T位于第四周期,其相关信息如下表:
元素 | 相关信息 |
X | 宇宙中最丰富的元素 |
Y | 其单质是空气中最主要的成分 |
Z | 地壳中含量最高的元素 |
W | 其原子质量数为23,中子数为12 |
R | 其最高价氧化物对应的水化物既能与强酸反应,也能与强碱反应 |
T | 其单质在空气中放置表面会变绿,其常见氧化物有两种,为黑色和砖红色 |
(1)YZWR四种元素的原子半径从大到小的顺序是___________(用元素符号表示)
(2)YX3的电子式为;X与Z形成一种18e-的分子,其结构式为_____________
(3)A是人体必需的常量元素,与W同主族,位于第四周期,其原子序数为___________
(4)R在元素周期表中的位置为___________
(5)T单质可与Y最高价氧化物对应水化物的稀溶液发生反应,该反应的离子方程式为__________

