题目内容
【题目】为了测定某有机物A的结构,做如下实验:
①将4.4g该有机物完全燃烧,生成 0.2mol CO2和3.6g水;
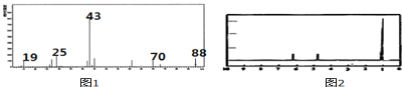
②用质谱仪测定其相对分子质量,得如图1的质谱图;③A的核磁共振氢谱如图2:
试回答下列问题:
(1)有机物A的相对分子质量是__________
(2)有机物A的分子式是_________
(3)有机物A的实验式是________
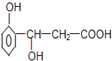
(4)红外光谱上发现A有﹣COOH和2个﹣CH3则有机物A的结构简式 ____________
【答案】88 C4H8O2 C2H4O ![]()
【解析】
(1)从图1的质谱图可知横坐标最大的吸收峰对应的数值为88,故有机物A的相对分子质量为88,故答案为:88;
(2)根据4.4g该有机物完全燃烧,生成0.2mol CO2和3.6g水可知,![]() ,n(C)=
,n(C)=![]() =0.2mol,
=0.2mol,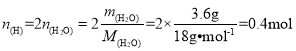 ,
,![]()
故:n(有机物):n(C):n(H):n(O)=0.05mol:0.2mol:0.4mol:0.1mol=1:4:8:2,故有机物A的分子式是C4H8O2,故答案为:C4H8O2;
(3)实验式是指有机物中各原子的最简整数比的式子,故有机物A的分子式为C4H8O2,故其实验式为C2H4O,故答案为:C2H4O;
(4)据红外光谱上发现A有﹣COOH和2个﹣CH3,结合有机物A的分子式为C4H8O2,则有机物A的结构简式为:![]() ,故答案为:
,故答案为:![]() 。
。

练习册系列答案
相关题目