题目内容
【题目】下列事实能用勒夏特列原理解释的是
A.工业上N2与H2合成NH3,往往需要使用催化剂
B.向1.50mol/L的硝酸铵溶液中加入少量氨水至中性,水的电离程度减小
C.密闭容器中2molCO与1molH2O(g)充分反应达平衡后,增大压强CO的反应速率加快
D.SO2与O2催化氧化成SO3是一个放热过程,450℃左右的温度比室温更有利于SO3生成
【答案】B
【解析】
勒夏特列原理适用的对象应存在可逆过程,如与可逆过程无关、与平衡移动无关,则不能用勒夏特列原理解释,合成氨工业中平衡移动使反应物转化率与产率提高,才可以用勒夏特列原理解释。
A. 合成氨的反应用铁触媒作催化剂,只能加快反应速率,不影响平衡移动,不能用勒夏特列原解释,故A错误;
B. 向1.50mol/L的硝酸铵溶液中加入少量氨水至中性,将抑制铵根离子水解,从而使水的电离程度减小,能用勒夏特列原理解释,故B正确;
C. 密闭容器中2molCO与1molH2O(g)发生反应:CO(g)+ H2O(g)![]() CO2(g)+H2(g),达到平衡后,增大压强CO的浓度增大,反应速率加快,但平衡不移动,不能用勒夏特列原解释,故C错误;
CO2(g)+H2(g),达到平衡后,增大压强CO的浓度增大,反应速率加快,但平衡不移动,不能用勒夏特列原解释,故C错误;
D. SO2与O2催化氧化成SO3是一个放热过程,从平衡移动的角度考虑,应该为降低温度有利于三氧化硫的生产,但是从催化剂活性考虑,450℃左右的温度比室温更有利于三氧化硫生成,不能用勒夏特列原解释,故D错误;
正确答案是B。

【题目】下列实验操作、现象及得出的结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 向盛有品红的两只试管中分别通入SO2和Cl2 | 品红均褪色 | 两者漂白原理相同 |
B | 向体积相同且pH均为3.3的一元酸HX和HY中分别加入足量锌粒 | 产生的H2前者比后者多 | HX、HY均是弱酸 |
C | 在难溶性FeS和CuS中分别加入0.3mol/L盐酸 | 前者溶解,后者不溶 | Ksp(FeS)>Ksp(CuS) |
D | 向盛有相同体积、10%H2O2溶液的两只试管中分别加入足量酸性KMnO4溶液和FeCl3溶液 | 前者产生的气体多 | KMnO4催化活性比FeCl3高 |
A. A B. B C. C D. D
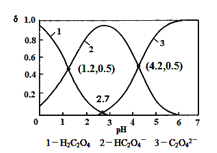
【题目】“中和滴定原理在实际生产生活中应用广泛某化学学习小组同学的研究课题是:探究测定草酸晶体(H2C2O4·xH2O)中的x值。通过查阅资和网络查寻,得知草酸易溶于水,其水溶液可以用酸性KMnO4溶液进行滴定,反应原理为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
回答下列问题:
(1)该滴定实验所需的玻璃仪器有______。
A.酸式滴定管(50mL) B.碱式滴定管(50mL) C.量筒(50mL) D.锥形瓶 E.烧杯
(2)滴定终点的现象为_____________________________________________________。
(3)某学生根据3次实验分别记录有关数据如下表:
滴定次数 | 待测H2C2O4溶液的体积/mL | 0.100mol·L-1KMnO4的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 滴液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
依据上表数据列式计算该H2C2O4溶液的物质的量浓度______________。(计算结果保留四位有效数字)
(4)讨论:若滴定到终点时俯视滴定管刻度线读数,则由此测得的x值会______________(填“偏大”、“偏小”或“不变”)。