题目内容
1.下列离子在水溶液中一定能大量共存的是( )| A. | K+ NH4+ HCO3- OH- | B. | Fe2+ H+ NO3- SO42- | ||
| C. | Na+ Cu2+ SO42- NO3- | D. | Al3+ Ba2+ CO32- Cl- |
分析 A.铵根离子、碳酸氢根离子都与氢氧根离子反应;
B.硝酸根离子在酸性条件下能够氧化亚铁离子;
C.四种离之间不发生反应,能够共存;
D.铝离子与碳酸根离子发生双水解反应,钡离子与碳酸根离子反应生成碳酸钡沉淀.
解答 解:A.NH4+、HCO3-都与OH-发生反应,在溶液中不能大量共存,故A错误;
B.Fe2+、H+、NO3-之间发生氧化还原反应,在溶液中不能大量共存,故B错误;
C.Na+、Cu2+、SO42-、NO3-之间不反应,在溶液中概念大量共存,故C正确;
D.Al3+、CO32-之间发生双水解反应生成氢氧化铝沉淀和二氧化碳气体,Ba2+、CO32-之间反应生成碳酸钡沉淀,在溶液中不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的正误判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间,能发生络合反应的离子之间(如 Fe3+和 SCN-)等;试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.今年是世界反法西斯战争暨中国人民抗日战争胜利70周年.二战期间日本是在战场上唯一大量使用毒气弹的国家.芥子气〔(ClCH2CH2)2S〕是其中一种毒气,即使嗅觉不能感受的极低浓度也会对人造成伤害,可用NaOH溶液解毒.芥子气可用以下方法制备:2CH2=CH2+S2Cl2→(ClCH2CH2)2S+S.下列有关说法正确的是
( )
( )
| A. | 芥子气不是烃的衍生物 | |
| B. | 芥子气可以和硝酸银溶液反应生成氯化银沉淀 | |
| C. | S2Cl2中有极性键和非极性键 | |
| D. | NaOH溶液解毒原理是酸碱中和反应 |
16.环境问题是全球共同关注的问题,环境污染的发生、危害与防治都与化学有关.根据有关的化学知识,下列说法正确的是( )
| A. | 严禁排放未经处理的有毒工业废水--防止水土流失 | |
| B. | 不允许焚烧农作物秸秆--防止温室效应 | |
| C. | 限制生产含磷洗涤剂--防止江河、湖泊出现“赤潮” | |
| D. | 限制生产不符合尾气排放标准的汽车--防止氮的氧化物及一氧化碳等污染空气 |
6.下列有关化学与生活的叙述错误的是( )
| A. | 利用太阳能、潮汐能、风力发电,可以获取清洁能源 | |
| B. | 常在包装袋内放入生石灰以防止月饼等富脂食品氧化变质 | |
| C. | 利用可降解的“玉米塑料”生产一次性饭盒,可防止白色污染 | |
| D. | 采用纳米二氧化钛光触媒技术可将汽车尾气中的NO和CO转化为无害气体 |
13.X、Y均为短周期元素,其简单离子aXn-和bYm+电子层结构相同,则下列说法正确的是( )
| A. | b-a=m+n | B. | X的原子半径大于Y | ||
| C. | X的族序数一定小于Y | D. | X不可能是氢元素 |
10.下列化学用语正确的是( )
| A. | 2-乙基-1,3-丁二烯分子的键线式: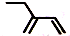 | B. | 丙烷分子的比例模型: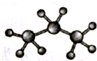 | ||
| C. | 四氯化碳分子的电子式: | D. | 聚丙烯的结构简式: |
18.在恒温下的密闭容器中,有可逆反应2NO(g)+O2(g)?2NO2(g)△H<0,其中NO为无色气体,NO2为红棕色气体.不能作为达到化学平衡状态标志的是( )
| A. | 正反应生成NO2的速率和逆反应生成O2的速率相等 | |
| B. | 混合气体颜色深浅保持不变 | |
| C. | 反应器中压强不随时间变化而变化 | |
| D. | 混合气体平均相对分子质量保持不变 |

 (1)氢能源是21世纪极具有发展前景的新能源之一,它既是绿色能源,又可循环使用.请在下图的每个空格中填上循环过程中反应物和生成物的分子式,以完成理想的氢能源循环体系图(循环中接受太阳能的物质在自然界中广泛存在):①H2O,②H2和O2.从能量转换的角度看,过程Ⅱ应是化学能转化为电能.
(1)氢能源是21世纪极具有发展前景的新能源之一,它既是绿色能源,又可循环使用.请在下图的每个空格中填上循环过程中反应物和生成物的分子式,以完成理想的氢能源循环体系图(循环中接受太阳能的物质在自然界中广泛存在):①H2O,②H2和O2.从能量转换的角度看,过程Ⅱ应是化学能转化为电能.