题目内容
18.在恒温下的密闭容器中,有可逆反应2NO(g)+O2(g)?2NO2(g)△H<0,其中NO为无色气体,NO2为红棕色气体.不能作为达到化学平衡状态标志的是( )| A. | 正反应生成NO2的速率和逆反应生成O2的速率相等 | |
| B. | 混合气体颜色深浅保持不变 | |
| C. | 反应器中压强不随时间变化而变化 | |
| D. | 混合气体平均相对分子质量保持不变 |
分析 当可能反应达到平衡状态时,同种物质的正逆反应速率相等,不同物质的正逆速率之比等于其化学计量数之比,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,注意选择判断平衡的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A.正反应生成NO2的速率和逆反应生成O2的速率相等,不等于化学计量数之比2:1,反应向逆反应进行,故A错误;
B.混合气体颜色深浅保持不变,说明二氧化氮的浓度不变,说明到达平衡状态,故B正确;
C.随反应进行,容器内压强减小,反应器中压强不随时间变化而变化说明到达平衡,故C正确;
D.混合气体总质量不变,随反应进行混合气体总物质的量减小,平均相对分子质量减小,混合气体平均相对分子质量保持不变说明到达平衡,故D正确,
故选A.
点评 本题考查化学平衡状态的判断,难度不大,注意理解化学平衡状态的特征,侧重考查学生的分析能力.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
1.下列离子在水溶液中一定能大量共存的是( )
| A. | K+ NH4+ HCO3- OH- | B. | Fe2+ H+ NO3- SO42- | ||
| C. | Na+ Cu2+ SO42- NO3- | D. | Al3+ Ba2+ CO32- Cl- |
6.如图所示的装置中,有关说法不正确的是( )
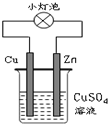

| A. | 该装置实现化学能转变为电能 | |
| B. | 该装置中Cu2+向Cu电极移动 | |
| C. | 该装置中Cu棒上Cu2+发生氧化反应析出Cu | |
| D. | 该装置中Zn棒上的电极反应为:Zn-2e-═Zn2+ |
13.甲、乙、丙、丁4种物质分别含有2种或3种元素,它们的分子中各含18个电子,甲是气态氢化物,在水中分步电离出的两种阴离子,下列推断合理的是( )
| A. | 某钠盐溶液含甲电离出的阴离子,则该溶液量碱性,只能与酸反应 | |
| B. | 乙与氧气的摩尔质量相同,则乙可能含极性键和非极性键 | |
| C. | 丙中含有第二周期IVA族元素,则丙一定是甲烷的同系物 | |
| D. | 丁和甲中各元素质量比相同,则丁中含有-2价的元素 |
10.有机物:①CH2OH(CHOH)4CHO ②CH3CH2CH2OH ③CH2=CHCHOHCH3 ④CH2=CH-COOCH3 ⑤CH2=CH-COOH ⑥CHCl=CH-COOH中能发生加成反应、酯化反应、氧化反应、还原反应、消去反应的是( )
| A. | ③⑤⑥ | B. | ①③⑥ | C. | ②④⑥ | D. | ①③⑤ |
7.下列有关结构中,C原子有可能处于同一平面上的最大组合是( )
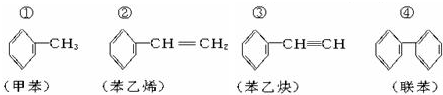

| A. | ①④ | B. | ②③ | C. | ①②④ | D. | 全部 |
8.下列说法正确的是( )
| A. | 物质发生化学反应都伴随着能量变化,但不一定会引起状态的变化 | |
| B. | 伴随着能量变化的物质变化都是化学变化 | |
| C. | 反应物的总能量低于反应产物的总能量,此反应需加热才进行 | |
| D. | 反应物的总能量高于反应产物的总能量,此反应在任何条件下都可进行 |
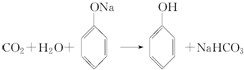
 +H2O.
+H2O.