题目内容
【题目】实验室需配制500mL0.2mol/LNaOH溶液,实验操作步骤为:
A.把制得的溶液小心地转移至容量瓶中。
B.在天平上称取 g的氢氧化钠钠固体,把它放在烧杯中,用适量的蒸馏水将它完全溶解并冷却至室温。
C.继续向容量瓶中加蒸馏水至 ,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切。
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心注入容量瓶,并轻轻振荡。
E.将容量瓶塞塞紧,充分摇匀。
请填写下列空白:
(1)操作步骤的正确顺序为___(填序号)。
(2)题目B、C项空白处填入。___、___。
(3)本实验用到的基本仪器已有烧杯、天平(砝码、镊子)、玻璃棒,还缺少的必要仪器是___。
(4)下列情况中,会使所配溶液浓度偏高的是___(填序号)。
A.没有冷却直接移液
B.没有进行上述的操作步骤D
C.加蒸馏水时,不慎超过了刻度线
D.容量瓶使用前内壁沾有水珠
【答案】BADCE 4.0 刻度线下1~2cm 500mL容量瓶 量筒 A
【解析】
(1)配制一定物质的量浓度的操作步骤包括:验漏→计算→称量→溶解→转移→洗涤→震荡→定容→摇匀→装液,故操作步骤的正确顺序为BADCE,故答案为:BADCE;
(2)配制500mL0.2mol/LNaOH溶液所需的固体NaOH的质量为:![]() ,定容时为防止直接加水太快而导致溶液超出刻度线,需要在加水到刻度线下1~2cm时改用胶头滴管,故答案为:4.0 刻度线下1~2cm
,定容时为防止直接加水太快而导致溶液超出刻度线,需要在加水到刻度线下1~2cm时改用胶头滴管,故答案为:4.0 刻度线下1~2cm
(3)用固体配溶液时所需主要仪器有:烧杯、天平(砝码、镊子)、玻璃棒、500ml容量瓶和量筒,故还缺少的必要仪器是500ml容量瓶和量筒,故答案为:500ml容量瓶和量筒;
(4)A.由于固体热胀冷缩比液体慢,故没有冷却直接移液将导致结果偏大,故A符合题意;
B.没有进行上述的操作步骤D,即没有洗涤操作,将导致结果偏小,故B不符合题意;
C.加蒸馏水时,不慎超过了刻度线,溶液体积偏大,将导致结果偏小,故C不符合题意;
D.容量瓶使用前内壁沾有水珠,因为配制过程中还要向容量瓶中加水,故对实验结果无影响,故D不符合题意;
故答案为:A。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】Ⅰ.某实验小组对H2O2的分解做了如下探究,将质量相同的粉末状和块状的MnO2分别加入盛有15 mL5%的H2O2溶液的大试管中,并用带火星的木条测试,下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据。
MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5 min |
块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30 min |
(1)写出大试管中发生反应的化学方程式:______。该反应是______(填“放热”或“吸热”)反应。
(2)实验结果表明,催化剂的催化效果与____有关。
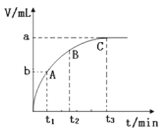
(3)某同学在10 mLH2O2溶液中加入一定量的MnO2,放出气体的体积(标准状况)与反应时间的关系如下图所示,则A、B、C三点所表示的反应速率最慢的是____。
Ⅱ.某反应在体积为5 L的恒容密闭容器中进行,在0~3分钟内各物质的量的变化情况如下图所示(A,B,C均为气体)。
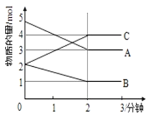
(4)该反应的化学方程式为____。
(5)反应开始至2分钟时,B的平均反应速率为_____,A的转化率为______。