题目内容
7.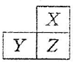 X,Y,Z是三种短周期的主族元素,在周期表的位置如图,X原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )
X,Y,Z是三种短周期的主族元素,在周期表的位置如图,X原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )| A. | 原子半径:X>Y>Z | |
| B. | 气态氢化物的热稳定性:X<Z | |
| C. | Y和Z的最高价氧化物对应水化物均为强酸 | |
| D. | X和Z形成的化合物只有共价键 |
分析 X、Y、Z是三种短周期的主族元素,由各元素在周期表中的位置可知,X处于第二周期,Y、Z处于第三周期,X原子的最外层电子数是其次外层电子数的3倍,原子只能有2个电子层,X最外层电子数为6,故X为O元素,则Z为S元素,Y为P元素,结合元素周期律进行解答.
解答 解:X、Y、Z是三种短周期的主族元素,由各元素在周期表中的位置可知,X处于第二周期,Y、Z处于第三周期,X原子的最外层电子数是其次外层电子数的3倍,原子只能有2个电子层,X最外层电子数为6,故X为O元素,则Z为S元素,Y为P元素.
A.同周期自左而右原子半径减小、同主族自上而下原子半径增大,故原子半径:Y>Z>X,故A错误;
B.同主族自上而下非金属性减弱,故非金属性X>Z,氢化物稳定性与元素非金属性一致,则氢化物稳定性X>Z,故B错误;
C.硫酸属于强酸,但磷酸属于中强酸,故C错误;
D.X与Z形成的化合物为二氧化硫、三氧化硫,只含有共价键,故D正确,
故选D.
点评 本题考查结构性质位置关系应用,难度不大,整体把握元素周期表是元素推断的关键,有利于基础知识的巩固.

练习册系列答案
 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
17.下列叙述正确的是( )
| A. | 在一定条件下通入氢气发生反应,可除去乙烷中混有的乙烯 | |
| B. | 苯能与溴发生取代反应,因此不能用苯萃取溴水中的溴 | |
| C. |  的一氯代物有4种 的一氯代物有4种 | |
| D. | 甲醛溶液与足量的银氨溶液共热的离子反应方程式为:HCHO+4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$CO32-+2NH4++4Ag↓+6NH3+2H2O |
18.下列有关实验的说法不正确的是( )
| A. | 测定中和热实验的玻璃仪器只需烧杯、量筒和温度计 | |
| B. | 用25mL碱式滴定管量取13.50mL Na2CO3溶液 | |
| C. | 用10mL量筒量取5.5mL硫酸溶液 | |
| D. | 用广泛pH试纸不能测得某碱溶液的pH为12.7 |
15.已知某有机物的结构简式如图所示,下列说法不正确的是( )
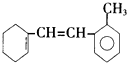
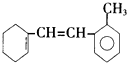
| A. | 分子式为C15H18 | |
| B. | 能使酸性KMnO4溶液褪色,且是氧化反应 | |
| C. | 1mol该物质最多和2molH2加成 | |
| D. | 苯环上的一氯化物有4种 |
12. 某温度时,在一个容积为2L的密闭容器中,X,Y,Z三种气体的物质的量随时间的变化曲线如图所示,根据图中数据,下列有关说法错误的是( )
某温度时,在一个容积为2L的密闭容器中,X,Y,Z三种气体的物质的量随时间的变化曲线如图所示,根据图中数据,下列有关说法错误的是( )
 某温度时,在一个容积为2L的密闭容器中,X,Y,Z三种气体的物质的量随时间的变化曲线如图所示,根据图中数据,下列有关说法错误的是( )
某温度时,在一个容积为2L的密闭容器中,X,Y,Z三种气体的物质的量随时间的变化曲线如图所示,根据图中数据,下列有关说法错误的是( )| A. | 反应开始至2min,Z的反应速率为0.10mol•L-1•min-1 | |
| B. | 该反应的化学方程式为3X+Y?2Z | |
| C. | 2min时,反应达最大限度,但化学反应仍在进行 | |
| D. | 反应达到平衡时,压强是开始时的0.9倍 |
19.下列有关有机物的说法错误的是( )
| A. | 乙烯、氯乙烯都可通过加聚反应合成塑料 | |
| B. | 油脂、糖和蛋白质都能发生水解反应 | |
| C. | 只用Cu(OH)2:悬浊液就可鉴别乙醇、乙醛和乙酸 | |
| D. | 苯分子中所有的原子都在同一平面上 |
16.将ag镁铁合金投入适量稀硝酸(假设NO是唯一的还原产物,不考虑溶解氧等其它氧化剂)中,当硝酸消耗完时收集到标准状况下2.24L的气体.然后向反应后的溶液中加入3mol•L-1NaOH溶液至金属恰好沉淀完全,沉淀质量为bg,则下列说法不正确的( )
| A. | 若在与硝酸反应后的溶液中再加入Fe,金属可能溶解 | |
| B. | 消耗的氢氧化钠的体积为100mL | |
| C. | b=a+5.1 | |
| D. | a的范围为:3.6<a<5.6 |
17.500mL KNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0mol/L,用石墨作电极电解此溶液,当通电一段时间后(假设溶液体积不变),两极均收集到22.4L气体(标准状况).下列说法正确的是( )
| A. | 上述电解过程中铜转移2mol电子 | B. | 电解后溶液中c(H+)为4mol/L | ||
| C. | 电解得到的Cu的物质的量为0.5mol | D. | 原混合溶液中c(K+)为1mol/L |
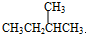 与
与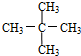 G.
G.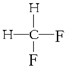 与
与