题目内容
【题目】在下列各溶液中,一定能大量共存的离子组是
A.常温下水电离的c(H+)为1×10-12mol/L的溶液中:Fe2+、Na+、SO42-、NO3-
B.滴加石蕊后呈蓝色的溶液中:K+、AlO2-、Cl-、HCO3-
C.使石蕊呈红色的溶液:NH4+、NO3﹣、AlO2﹣、I﹣
D.常温下![]() =1014的溶液中:K+、Ba2+、Cl-、Br-
=1014的溶液中:K+、Ba2+、Cl-、Br-
【答案】D
【解析】
A. 常温下水电离的![]() 为1×1012mol/L的溶液,为酸或碱溶液,酸溶液中
为1×1012mol/L的溶液,为酸或碱溶液,酸溶液中![]() 发生氧化还原反应不能大量共存,碱溶液中不能大量存在
发生氧化还原反应不能大量共存,碱溶液中不能大量存在![]() ,故A不符合题意;
,故A不符合题意;
B. 滴加石蕊后呈蓝色的溶液,显碱性,不能大量存在![]() ,且
,且![]() 与
与![]() 反应生成氢氧化铝和CO32-不能大量共存,故B不符合题意;
反应生成氢氧化铝和CO32-不能大量共存,故B不符合题意;
C. 使石蕊变红的溶液显酸性,![]() 和氢离子反应不能大量存在,故C不符合题意;
和氢离子反应不能大量存在,故C不符合题意;
D. 常温下![]() =1014的溶液显碱性,该组离子之间不反应,可大量共存,故D符合题意;
=1014的溶液显碱性,该组离子之间不反应,可大量共存,故D符合题意;
答案选D。

【题目】某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液。
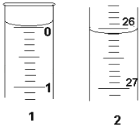
(1)若滴定开始和结束时,酸式滴定管中的液面如图所示:则所用盐酸的体积为__mL。滴定终点时的现象是:当滴入最后一滴盐酸时,锥形瓶中溶液颜色由___,且30s不恢复原色。
(2)某学生根据三次实验分别记录有关数据如下表:
滴定次数 | 待测氢氧化钠 溶液的体积/mL | 0.1000mol·L-1盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积 | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
请选用其中合理数据算出该氢氧化钠溶液物质的量浓度(计算结果保留4位有效数字):c(NaOH)=__mol·L-1。
(3)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是__(填字母)。
A.滴定前滴定管中有气泡,滴定后消失 B.碱式滴定管量取NaOH溶液时,未进行润洗操作
C.滴定时达到滴定终点时俯视读数 D.锥形瓶取用NaOH待测液前加少量水洗涤
【题目】根据要求回答下列有关问题。
(1)甲醇是一种重要的化工原料,工业上利用CO2和H2在一定条件下反应合成甲醇。已知:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1=-1275.6kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566.0kJ·mol-1
③H2O(g)=H2O(l) ΔH3=-44.0kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:___。
(2)高炉炼铁是冶炼铁的主要方法,发生的主要反应为:Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g) H=-28.5kJ/mol,冶炼铁反应的平衡常数表达式K=__,温度升高后,K值__(填“增大”、“不变”或“减小”)。
2Fe(s)+3CO2(g) H=-28.5kJ/mol,冶炼铁反应的平衡常数表达式K=__,温度升高后,K值__(填“增大”、“不变”或“减小”)。
(3)在T℃时,反应Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g)的平衡常数K=64,在2L恒容密闭容器中,按下表所示加入物质,经过一段时间后达到平衡。
2Fe(s)+3CO2(g)的平衡常数K=64,在2L恒容密闭容器中,按下表所示加入物质,经过一段时间后达到平衡。
Fe2O3 | CO | Fe | CO2 | |
始态mol | 1.0 | 1.0 | 1.0 | 1.0 |
①平衡时CO 的转化率为___。
②下列情况标志反应达到平衡状态的是__(填字母)。
a.容器内气体密度保持不变
b.容器内气体压强保持不变
c.CO的消耗速率和CO2的生成速率相等
d.容器内气体的平均相对分子质量保持不变