题目内容
19.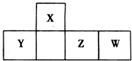 短周期元素X、Y、Z、W在周期表中的相对位置如图,X的气态氢化物能与其最高价氧化物对应的水化物反应生成盐.下列判断错误的是( )
短周期元素X、Y、Z、W在周期表中的相对位置如图,X的气态氢化物能与其最高价氧化物对应的水化物反应生成盐.下列判断错误的是( )| A. | 最简单气态氢化物的稳定性:X>Y | |
| B. | 单核阴离子半径:Z>W | |
| C. | 含Z元素的盐溶液可能显酸性、碱性或中性 | |
| D. | W元素的单质具有漂白性,常用于自来水的杀菌消毒 |
分析 短周期元素中,X的气态氢化物能与其最高价氧化物对应的水化物反应生成盐,则X为N元素,由元素X、Y、Z、W在周期表中的相对位置,可知Y为Si、Z为S、W为Cl.
A.同周期自左而右元素非金属性增强、同主族自上而下元素非金属性减弱,非金属性越强,氢化物越稳定;
B.电子层结构相同的两种,核电荷数越大离子半径越小,电子层越多离子半径越大;
C.硫酸钠溶液为中性、硫酸为酸性、亚硫酸钠溶液为碱性;
D.氯气没有漂白性,但氯气与水反应得到HClO起漂白作用.
解答 解:短周期元素中,X的气态氢化物能与其最高价氧化物对应的水化物反应生成盐,则X为N元素,由元素X、Y、Z、W在周期表中的相对位置,可知Y为Si、Z为S、W为Cl.
A.同周期自左而右元素非金属性增强、同主族自上而下元素非金属性减弱,故非金属性X>Y,非金属性越强,氢化物越稳定,则最简单气态氢化物的热稳定性为X>Y,故A正确;
B.S2-、Cl-离子电子层结构相同,核电荷数越大离子半径越小,故离子半径:S2->Cl-,故B正确;
C.Z为硫元素,其化合物中硫酸钠溶液为中性、硫酸为酸性、亚硫酸钠溶液为碱性,故C正确;
D.氯气处于用于自来水杀菌消毒,但氯气没有漂白性,是氯气与水反应得到HClO起漂白作用,故D错误,
故选:D.
点评 本题考查元素周期表和元素周期律,X为推断的突破口,明确元素在周期表中的位置及性质变化规律即可解答,题目难度中等.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
10.常温下,下列有关叙述正确的是( )
| A. | 在0.1mol•L-1Na2C2O4溶液中:2c(Na+)=c(C2O42-)+c(HC2O4-)+c(H2C2O4) | |
| B. | 向10mL pH=12的NaOH溶液中滴加等体积pH=2的CH3COOH溶液:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) | |
| C. | 浓度均为0.1 mol•L-1的小苏打溶液与烧碱溶液等体积混合:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-) | |
| D. | 浓度均为0.1 mol•L-1的硫酸氢铵溶液与氢氧化钠溶液等体积混合c(SO42-)=c(Na+)>c(NH4+)>c(H+)>c(OH-) |
10.下列装置能达到对应实验目的是( )
| A. |  分离碘与沙子 | B. | 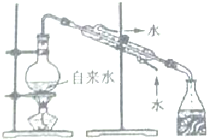 实验室制取蒸馏水 | ||
| C. | 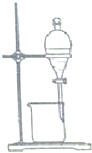 乙醇提取碘水中的碘 | D. | 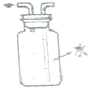 收集氨气 |
14.只用一种试剂就能将甲苯、己烯、四氯化碳和碘化钾溶液区分开,该试剂可以是( )
| A. | 酸性高锰酸钾溶液 | B. | 溴化钠溶液 | ||
| C. | 溴水 | D. | 硝酸银溶液 |
4.下列说法不正确的是( )
| A. | 乙醇可由淀粉、纤维素等在一定条件下制得 | |
| B. | 乙醇、乙酸生成乙酸乙酯的反应属于取代反应 | |
| C. | 乙醇可与NaOH稀溶液反应 | |
| D. | 乙醇与二甲醚(CH3 OCH3)是同分异构体 |
11.X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示.Z为地壳中含量最多的金属元素,下列说法中正确的是( )
| X | Y | |||
| Z | W | Q |
| A. | X、Y、W三种元素最低价氢化物的沸点依次升高 | |
| B. | 原子半径:Q>W>Z>Y>X | |
| C. | 最高价氧化物对应水化物的酸性:Q>W>Z | |
| D. | X及Q的气态氢化物相反应,形成的化合物为离子化合物 |
7.常温下,在下列指定条件的各溶液中,一定能大量共存的离子组是( )
| A. | 含0.1 molL-1SO2的溶液中:Na+、Ba2+、Br-、Cl- | |
| B. | 能与金属铝反应放出氢气的溶液中:K+、Mg2+、NO${\;}_{3}^{-}$、SiO${\;}_{3}^{2-}$ | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=10-12的溶液中:K+、NH${\;}_{4}^{+}$、SO${\;}_{4}^{2-}$、NO${\;}_{3}^{-}$ | |
| D. | 不能使酚酞变红的无色溶液中:Na+、K+、ClO-、I- |
6.下列说法或表示方法正确的是( )
| A. | 凡是吸热或放热过程中热量的变化均称为反应热 | |
| B. | 热化学方程式中的化学计量数只表示物质的量,可以是分数 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷燃烧热 |
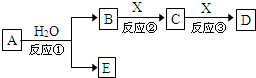 由短周期元素组成的中学常见物质A、B、C、D、E存在图转化关系(部分生成物和反应条件略).
由短周期元素组成的中学常见物质A、B、C、D、E存在图转化关系(部分生成物和反应条件略).