题目内容
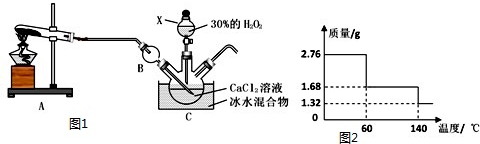
3.过氧化钙(CaO2)是一新型的多功能无机化工产品,常温下为无色或淡黄色粉末,易溶于酸,难溶于水、乙醇等有机溶济.某实验小组在实验室用钙盐制取CaO2•8H2O 沉淀(该反应是一个放热反应).(1)仪器X的名称是:分液漏斗.
(2)仪器B的作用是:防止倒吸.
(3)图1验室制取氨气的装置,写出A中发生反应的化学方程式:2NH4Cl+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(4)制取CaO2•8H2O一般在0-5℃的低温下进行,原因是:低于0℃,液体易冻结,反应困难,温度较高,过氧化氢分解速率加快,生成CaO2•8H2O的化学方程式为:CaCl2+H2O2+2NH3+8H2O=CaO2•8H2O+2NH4Cl.
(5)2.76g CaO2•8H2O样品(含杂质)受热脱水过程的热重曲线(样品质量随温度变化曲线,140℃进完全脱水,杂质受热不分解)如图2所示.
①试确定60℃时CaO2•xH2O中x=2.
②该样品中CaO2的质量分数为:26.09%.
分析 (1)根据X的特征可知为分液漏斗;
(2)氨气极易溶于水,防止倒吸;
(3)实验室中用氯化铵和氢氧化钙固体制取氧气;
(4)低于O℃,液体易冻结,反应困难,温度过高,过氧化氢分解速率加快,CaCl2与H2O2、NH3、H2O反应生成CaO2•8H2O与NH4Cl;
(5)①140℃时完全脱水,杂质受热不分解,结合样品总质量计算出结晶水的总质量、物质的量,从而得出样品中CaO2•8H2O物质的量,再根据60℃时固体的质量计算出失去结晶水的质量、物质的量,进而计算出CaO2•xH2O中的x;
②根据①计算出的样品中CaO2的物质的量,根据m=nM计算出其质量,再计算出样品中CaO2•8H2O的纯度.
解答 解:(1)根据X的特征可知X为分液漏斗,
故答案为:分液漏斗;
(2)A中产生的氨气极易溶于C中,B装置可以防倒吸,
故答案为:防倒吸;
(3)实验室中用氯化铵和氢氧化钙固体制取氧气,反应方程式为:Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,
故答案为:Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
(4)由于低于0℃,液体易冻结,反应困难,而温度较高,过氧化氢分解速率加快,所以制取CaO2•8H2O一般在0℃~5℃的低温下进行;
生成CaO2•8H20的化学方程式为:CaCl2+H2O2+2NH3+8H2O=2NH4Cl+CaO2•8H2O,
故答案为:低于0℃,液体易冻结,反应困难,温度较高,过氧化氢分解速率加快;CaCl2+H2O2+2NH3+8H2O=2NH4Cl+CaO2•8H2O;
(5)①140℃时完全脱水,杂质受热不分解,则样品中CaO2•8H2O含有的结晶水的总质量为:2.76g-1.32g=1.44g,结晶水的物质的量为:$\frac{1.44g}{18g/mol}$=0.08mol,原样品中含有CaO2•8H2O的物质的量为:$\frac{0.08mol}{8}$=0.01mol,
60℃时固体的质量为1.68g,失去结晶水的质量为:2.76g-1.68g=1.08g,失去结晶水的物质的量为:$\frac{1.08g}{18g/mol}$=0.06mol,故60℃时CaO2•xH2O中x=$\frac{0.08mol-0.6mol}{0.01mol}$=2,
故答案为:2;
②根据①可知CaO2•8H2O的物质的量为0.01mol,则CaO2的物质的量也是0.01mol,其质量为:72g/mol×0.01mol=0.72g,样品中CaO2的纯度为:$\frac{0.72g}{2.76g}$×100%≈26.09%,
故答案为:26.09%.
点评 本题考查实验方案的设计、物质组成及含量测定计算,题目难度中等,充分考查学生的分析理解能力、知识迁移应用能力.

 阅读快车系列答案
阅读快车系列答案| A. | 3:2:1 | B. | 6:3:2 | C. | 9:3:1 | D. | 12:6:5 |
| A. | 28g氮气含有的原子数为NA | |
| B. | 32 g O2中所含的氧原子数目为2NA | |
| C. | 2.7g金属铝与足量盐酸反应时失去的电子数为0.1NA | |
| D. | 标准状况下22.4L水所含的分子数为NA |
| A. | 中子数为16的磷原子:${\;}_{15}^{31}$P | |
| B. | 质子数为17的氯原子:${\;}_{17}^{35}$Cl | |
| C. | 质量数为57的铁原子:${\;}_{57}^{26}$Fe | |
| D. | 核外电子数为16的硫原子:${\;}_{16}^{32}$S |