题目内容
【题目】对于反应A(g)+4B(g)![]() 2C(g)+2D(g),下列数据表示反应进行得最快的是( )
2C(g)+2D(g),下列数据表示反应进行得最快的是( )
A.v(A)=1.4mol/(Ls)B.v(B)=3.6 mol/(Ls)
C.v(C)=2mol/(Ls)D.v(D)=30 mol/(Lmin)
【答案】A
【解析】
在相同条件下,同一化学反应中,用不同的物质表示化学反应速率其数值不同,但其数值之比等于化学计量数之比,即![]() ,因此在比较反应速率快慢时,先转化为同一种物质,以B的反应速率为标准进行判断。
,因此在比较反应速率快慢时,先转化为同一种物质,以B的反应速率为标准进行判断。
A. v(A)=1.4mol/(Ls),反应速率之比等于其化学计量数之比,所以v(B)=4v(A)=5.6mol/(Ls);
B. v(B)=3.6mol/(Ls);
C. v(C)=2mol/(Ls),反应速率之比等于其化学计量数之比,所以v(B)=2v(C)=4mol/(Ls);
D. v(D)=30mol/(Lmin)=0.5mol/(Ls),反应速率之比等于其化学计量数之比,所以v(B)= 2v(D)=1mol/(Ls);
所以反应速率最快的为A;
答案选A。

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案【题目】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
第二周期 | ① | ② | ||||||
第三周期 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
第四周期 | ⑧ | ⑨ |
(1)在这些元素中,化学性质最不活泼的是:_________(填元素符号)。
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的分子式是:_________,碱性最强的化合物的电子式是:_________。
(3)元素⑤的单质与元素③的最高价氧化物对应的水化物反应的离子方程式为_________。
(4)元素②的简单氢化物是由_________ (填“极性”或“非极性”)键形成的,在常温下该化合物与元素⑥的单质反应的离方程式为__________________。
(5)元素②、③、⑥、⑧四种元素形成的离子,离子半径由大到小的顺序是_________ (用离子符号表示)。
【题目】H2C2O4为二元弱酸。回答下列问题:
(1)20℃时,配制一组c(H2C2O4)+c(HC2O4-)+ c(C2O42-)=0.100 mol·L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如下图所示。
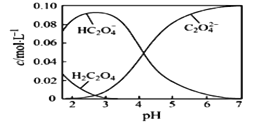
①H2C2O4的电离方程式为___________。
②为获得尽可能纯的NaHC2O4,pH应控制在_______左右。
③NaHC2O4溶液呈酸性,其原因为_________________。
④pH=6时,溶液中含碳微粒浓度大小关系为_______________。
(2)常温下,草酸、碳酸的电离平衡常数如下:
化学式 | H2CO3 | H2C2O4 |
平衡常数 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka1=5.6×10-2 Ka2=5.4×10-5 |
①常温下,0.1 mol·L-1 Na2CO3溶液的pH____0.1 mol·L-1 Na2C2O4溶液的pH。(填“>”、“<”或“=”)
② pH=4的H2C2O4溶液中c(C2O42-):c(HC2O4-)=_________。