题目内容
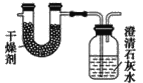
【题目】已知某种燃料含有碳、氢、氧三种元素。为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的O2中燃烧,并使产生的气体全部通过如图所示装置中,得到如表中所列的实验结果(假设产生的气体完全被吸收)。

根据实验数据求:
(1)实验完毕后,生成物中水的质量为________g。假设广口瓶里生成一种正盐,其质量为_____________g。
(2)生成的水中氢元素的质量为_______g。
(3)生成的二氧化碳中碳元素的质量为_______ g。
(4)该燃料中碳元素与氢元素的质量比为_______。
(5)已知这种燃料的每个分子中含有一个氧原子,则该燃料的分子式为_______,结构简式为_______。
【答案】1.8 5 0.2 0.6 3∶1 CH4O CH3OH
【解析】
(1)因为该燃料含C、H、O三种元素,故燃烧产物为CO2和H2O,由题意可知U形管增加的质量为吸收水的质量,广口瓶增加的质量为生成的CO2质量,生成的正盐为CaCO3,根据碳原子守恒计算CaCO3的物质的量,再根据m=nM计算CaCO3的质量;
(2)根据水的分子式中H元素质量分数计算;
(3)根据碳元素守恒、结合m=nM计算二氧化碳中C元素质量;
(4)由元素守恒,结合(2)(3)中的数据计算;
(5)确定化合物中C、H原子数目比,结合每个分子中含有一个O原子,确定该燃料的分子式、结构简式。
(1)由题意知,燃料燃烧生成的H2O和CO2分别被干燥剂和澄清石灰水吸收,二者的增重量即为燃烧时产生的H2O和CO2的质量。
(1)m(H2O)=102.9 g-101.1 g=1.8 g,m(CO2)=314.2 g-312.0 g=2.2 g。反应生成的正盐CaCO3质量为m(CaCO3)=![]() =5g;
=5g;
(2)m(H)=![]() =0.2 g
=0.2 g
(3)m(C)=![]() =0.6 g
=0.6 g
(4)m(C)∶m(H)=0.6 g∶0.2 g=3∶1
(5)燃料中n(C)∶n(H)=![]() ∶
∶![]() =1∶4,由于该燃料中H原子已达饱和,则该燃料的每个分子中只含有一个C原子,H原子数目为4,结合每个分子中含有一个O原子,所以该燃料的分子式为CH4O,结构简式为CH3OH。
=1∶4,由于该燃料中H原子已达饱和,则该燃料的每个分子中只含有一个C原子,H原子数目为4,结合每个分子中含有一个O原子,所以该燃料的分子式为CH4O,结构简式为CH3OH。

 优学名师名题系列答案
优学名师名题系列答案