题目内容
【题目】已知0.1 mol/L的氨水溶液中存在电离平衡:NH3·H2O![]() NH4++OH-,对于该平衡,下列叙述正确的是
NH4++OH-,对于该平衡,下列叙述正确的是
A. 加入水时,平衡向逆反应方向移动
B. 加入少量NaOH固体,平衡向正反应方向移动
C. 加入少量0.1 mol/LHCl溶液,溶液中c(OH-)减小
D. 加入少量NH4Cl固体,平衡向正反应方向移动
【答案】C
【解析】A.加水促进弱电解质的电离,则电离平衡正向移动,故A错误;B.向氨水中加入少量氢氧化钠固体,溶液中氢氧根离子浓度增大,平衡向逆反应方向移动,故B错误;C.向氨水中加入少量0.1 mol/LHCl溶液,氢离子和氢氧根离子反应生成水,所以氢氧根离子浓度减小,故C正确;D.加入少量NH4Cl固体,c(NH4+)增大,电离平衡逆向移动,故D错误;故选C。

练习册系列答案
相关题目
【题目】下列物质与水反应生成强碱的是( )
A. NH3 B. Na2O C. CO2 D. NO2
【答案】B
【解析】
A. NH3溶于水生成一水合氨,属于弱碱,A错误;B. Na2O溶于水生成氢氧化钠,是强碱,B正确;C. CO2溶于水生成碳酸,属于弱酸,C错误;D. NO2溶于水生成硝酸和NO,硝酸是强酸,D错误,答案选B。
【题型】单选题
【结束】
19
【题目】利用下列装置可以完成的实验组合是
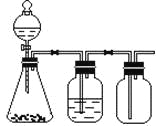
选项 | 制气装置 | 洗气瓶中试剂 | 瓶中气体 |
A | 氯酸钾 MnO2 | 浓硫酸 | O2 |
B | 石灰石 稀盐酸 | NaHCO3溶液 | CO2 |
C | Zn 稀硫酸 | 浓硫酸 | H2 |
D | MnO2 浓盐酸 | 浓硫酸 | Cl2 |
A. AB. BC. CD. D