题目内容
1.下列反应的离子方程式正确的是( )| A. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 氢氧化钡溶液跟稀硫酸反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | 铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 过氧化钠与水反应:2Na2O2+2H2O═4Na++4OH-+O2↑ |
分析 A.电荷不守恒;
B.该反应中氢氧根离子、氢离子和水的计量数都是2;
C.稀硫酸具有弱氧化性,能将变价金属氧化为较低价态;
D.二者反应生成氢氧化钠和氧气.
解答 解:A.电荷不守恒,离子方程式为2Na+2H2O═2Na++2OH-+H2↑,故A错误;
B.该反应中氢氧根离子、氢离子和水的计量数都是2,离子方程式为Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故B错误;
C.稀硫酸具有弱氧化性,能将变价金属氧化为较低价态,离子方程式为Fe+2H+═Fe2++H2↑,故C错误;
D.二者反应生成氢氧化钠和氧气,离子方程式为2Na2O2+2H2O═4Na++4OH-+O2↑,故D正确;
故选D.
点评 本题考查离子方程式正误判断,为高频考点,涉及氧化还原反应、复分解反应,离子方程式书写要遵循原子守恒、电荷守恒、转移电子守恒及化学反应规律,易错选项是C.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
12.下列物质中,不属于高分子化合物的是( )
| A. | 纤维素 | B. | 蛋白质 | C. | 油脂 | D. | 淀粉 |
9.为了维持生命和健康,人要从食物中摄取营养素,下列物质中不属于营养素的是( )
| A. | 葡萄糖 | B. | 蛋白质 | C. | 乙醇 | D. | 芝麻油 |
16.在强酸性无色透明溶液中,下列各组离子能大量共存的是( )
| A. | Cu2+、K+、Cl-、NO${\;}_{3}^{-}$ | B. | Ag+、Na+、NO${\;}_{3}^{-}$、Cl- | ||
| C. | Na+、Al3+、SO${\;}_{4}^{2-}$、Cl- | D. | Ba2+、NH${\;}_{4}^{+}$、Cl-、HCO${\;}_{3}^{-}$ |
6.质量都为4.2g的A气体和B气体,在标准状况下的体积分别为2.94L和3.36 L,则这两种气体的摩尔质量之比为( )
| A. | 1:1 | B. | 15:13 | C. | 7:8 | D. | 8:7 |
11.下列实验操作或记录正确的是( )
| A. | 常温常压下测得1 mol N2的质量为28 g | |
| B. | 用量筒测得排水法收集到的氢气体积为50.28 mL | |
| C. | 用两只250 mL的容量瓶配制0.1 mol/L 500 mL的NaOH溶液 | |
| D. | 用托盘天平称得2.5 g胆矾,受热充分失水后,固体质量减轻0.9 g |
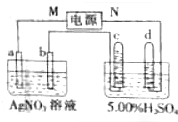 如图中电极a为Ag,电极b为Pt,电极c、d都是石墨电极.通电一段时间后,发现只有c、d两极上有气体产生,且标准状况下共收集到336mL气体.据此回答:
如图中电极a为Ag,电极b为Pt,电极c、d都是石墨电极.通电一段时间后,发现只有c、d两极上有气体产生,且标准状况下共收集到336mL气体.据此回答: