题目内容
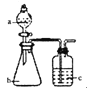
【题目】用如图所示装置和相应试剂能达到实验目的是:
选项 | 实验目的 | 试剂a | 试剂b | 试剂c | 装置 |
A | 验证非金属性:S>C>Si | 稀硫酸 | Na2CO3 | Na2SiO3溶液 |
|
B | 制备纯净的氯气 | 浓盐酸 | MnO2 | 饱和食盐水 | |
C | 检验溶液X中含有CO32- | 盐酸 | 溶液X | 澄清石灰水 | |
D | 除去Na2CO3中的Na2SO4 | 氯水 | 混合物 | NaOH溶液 |
A. A B. B C. C D. D
【答案】A
【解析】A、装置b中出现气体,说明硫酸的酸性强于碳酸,装置c中出现沉淀,说明碳酸的酸性强于硅酸,最高价氧化物对应水化物的酸性越强,非金属性越强,即S>C>Si,故正确;B、MnO2和浓盐酸反应,需要加热,此装置中没有加热装置,饱和食盐水除去氯气中的HCl,从装置c中出来氯气中混有水蒸气,不是纯净的,故错误;C、装置b中加入盐酸,出现能使澄清石灰水变浑浊的气体,不能说明X中含有CO32-,可能含有HCO3-或SO32-或HSO3-,故错误;D、氯水具有强氧化性,能把SO32-氧化成SO42-,不能达到实验目的,故错误。

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案
相关题目
【题目】由右表提供数据及相关物质结构知识,反应:SiCl4(g)+2H2(g)→Si(s)+4HCl(g),生成1mol
晶体硅的热效应是
化学键 | Si-Cl | H-H | Si-Si | H-Cl |
键能(kJ/mol) | 360 | 436 | 176 | 431 |
A.吸收236kJB.放出236kJC.放出116kJD.吸收116kJ