题目内容
10.下列说法正确的是( )| A. | 选择萃取剂将碘从碘水中萃取出来,这种萃取剂应具备的性质是不溶于水,且比水的密度大 | |
| B. | 选择萃取剂将碘从碘水中萃取出来,这种萃取剂应具备的性质是不溶于水,且比水的密度小 | |
| C. | 在使用分液漏斗进行分液时,上层液体经漏斗下口放出 | |
| D. | 选择萃取剂将碘从碘水中萃取出来,碘在四氯化碳中的溶解度比在水中的溶解度大 |
分析 A.选择萃取剂,不需要考虑密度;
B.萃取剂与水不互溶,且不能发生反应;
C.分液时,避免上下层液体混合;
D.碘不易溶于水,易溶于四氯化碳.
解答 解:A.选择萃取剂将碘从碘水中萃取出来,这种萃取剂应具备的性质是不溶于水,萃取剂的密度可大于水的密度或小于水的密度,故A错误;
B.选择萃取剂将碘从碘水中萃取出来,这种萃取剂应具备的性质是不溶于水,萃取剂的密度可大于水的密度或小于水的密度,如萃取剂为苯或四氯化碳,故B错误;
C.在使用分液漏斗进行分液时,先从下口分离出下层液体,再从上口分离出上层液体,故C错误;
D.选择萃取剂将碘从碘水中萃取出来,因碘在四氯化碳中的溶解度比在水中的溶解度大,则选择四氯化碳作萃取剂,故D正确;
故选D.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质及常见的混合物分离提纯方法的选择为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
1.下列措施,对增大反应速率明显有效的是( )
| A. | Na与水反应时增大水的用量 | |
| B. | Al在氧气中燃烧生成Al2O3,将铝片改成铝粉 | |
| C. | 在K2SO4与BaCl2两溶液反应时,增大压强 | |
| D. | Fe与硫酸反应制取H2时,选用浓硫酸 |
18.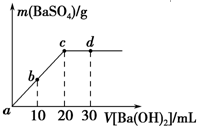 常温下,向0.25mol•L-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中不正确的是( )
常温下,向0.25mol•L-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中不正确的是( )
 常温下,向0.25mol•L-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中不正确的是( )
常温下,向0.25mol•L-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中不正确的是( )| A. | 硫酸溶液的体积为20mL | |
| B. | b时刻溶液中SO${\;}_{4}^{2-}$的浓度约为0.083mol•L-1 | |
| C. | d时刻溶液的pH为12 | |
| D. | 反应的离子反应方程式为Ba2++SO4-+2H++2OH-═BaSO4↓+2H2O |
15.下列各组离子在透明溶液中能大量共存的是( )
| A. | K+、Cu2+、Na+、Cl- | B. | H+、Na+、NO3-、CO32- | ||
| C. | Ba2+、H+、NO3-、SO42- | D. | Mg2+、Na+、OH-、SO42- |
2.下列四样溶液中,c(H+)浓度最大的是( )
| A. | 50mL 1.0mol/L的HCl | B. | 10mL 2.0mol/L 的NaCl | ||
| C. | 20mL 1.5mol/L 的HNO3 | D. | 10mL 1.0mol/L的H2SO4 |