题目内容
14.下列科学家对发现元素周期律贡献最大的是( )| A. | 拉瓦锡 | B. | 道尔顿 | C. | 阿伏加德罗 | D. | 门捷列夫 |
分析 1869年,俄国化学家门捷列夫发现了元素周期律,并编制出元素周期表,使得化学学习和研究变得有规律可循.
解答 解:A.拉瓦锡通过实验得出空气是由氧气和氮气组成的结论,故A错误;
B.道尔顿提出了近代原子学说,故B错误;
C.阿佛加德罗提出了分子学说,故C错误;
D.俄国化学家门捷列夫发现了元素周期律,并编制出元素周期表,使得化学学习和研究变得有规律可循,故D正确.
故选D.
点评 本题主要考查了化学史,难度不大,平时注意知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.等物质的量的乙烷、乙烯、乙炔完全燃烧消耗氧气的物质的量之比为( )
| A. | 1:1:1 | B. | 30:35:42 | C. | 5:4:3 | D. | 7:6:5 |
5.下列说法正确的是( )
| A. | 室温下,在水中的溶解度:乙醇>苯酚>乙酸乙酯 | |
| B. | 乙二醇和丙三醇互为同系物 | |
| C. | 分子式为C7H8O且属于酚类物质的同分异构体有4种 | |
| D. | 甲苯能使酸性高锰酸钾溶液褪色,说明甲基使苯环变活泼 |
2.四种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
试回答下列问题:(用相关元素符号、化学式等化学用语回答)
(1)元素Z位于周期表中第三周期VA族.
(2)这些元素的最简单氢化物中,相同条件下最易溶于水的是NH3(写化学式),写出该最简单氢化物与该元素的最髙价氧化物的水化物反应的离子方程式NH3+H+=NH4+.
(3)XW2的电子式为 .
.
(4)W的最高价氧化物的化学式为SO3;Y的一种氧化物YO2对环境的危害有光化学烟雾(任意写一种),试写出Y02与水反应的化学方程式3NO2+H2O=2HNO3+NO
(5)Z形成的四核单质分子形状是正四面体,其晶体类型是分子晶体;其晶体内部存在的微
粒间相互作用有分子间作用力、共价键.
| X | Y | |
| Z | W |
(1)元素Z位于周期表中第三周期VA族.
(2)这些元素的最简单氢化物中,相同条件下最易溶于水的是NH3(写化学式),写出该最简单氢化物与该元素的最髙价氧化物的水化物反应的离子方程式NH3+H+=NH4+.
(3)XW2的电子式为
 .
.(4)W的最高价氧化物的化学式为SO3;Y的一种氧化物YO2对环境的危害有光化学烟雾(任意写一种),试写出Y02与水反应的化学方程式3NO2+H2O=2HNO3+NO
(5)Z形成的四核单质分子形状是正四面体,其晶体类型是分子晶体;其晶体内部存在的微
粒间相互作用有分子间作用力、共价键.
9.下列说法正确的是( )
| A. | 某烯烃与氢气加成得2,2-二甲基丁烷,该烯烃是2,2-二甲基-1-丁烯 | |
| B. | 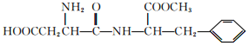 能发生水解反应,且与酸、碱均能反应 能发生水解反应,且与酸、碱均能反应 | |
| C. | 合成纤维、人造纤维及碳纤维都属于有机高分子材料 | |
| D. | 为检验某卤代烃中的卤素原子,应取少量卤代烃于试管中加入氢氧化钠溶液煮沸,冷却后加硝酸银溶液,然后根据卤化银沉淀的颜色确定卤素原子 |
19.一定条件下,在密闭容器中进行合成氨反应:N2(g)+3H2(g)?2NH3(g),当正、逆反应速率相等且不等于零时,下列说法不正确的是( )
| A. | N2、H2、NH3在容器中共存 | B. | N2、H2、NH3的浓度不改变 | ||
| C. | 反应已达到化学平衡状态 | D. | N2、H2完全转化为NH3 |
6.甲、乙、丙、丁4位同学分别设计了如下4个实验说明影响化学反应快慢的因素,结论不正确的是( )
| A. | 将浓硝酸分别放在冷暗处和强光照射卞,会发现光照可以加快浓硝酸的分解 | |
| B. | 将形状、大小均相同的镁条和铝条与相同浓度的盐酸反应时,两者速率一样 | |
| C. | 在相同条件下,等质量的大理石块和大理石粉末与相同浓度的盐酸反应,大理石粉末反应快 | |
| D. | 两只试管中分别加入相同质量的氯酸钾,其中一只试管中再加入少量二氧化锰,同时加热,加入二氧化锰的试管中产生氧气快 |
4.常温下,下列有关叙述正确的是( )
| A. | 0.1 mol•L-1 pH为4的KHC2O4溶液中:c(HC2O4-)>c(H2C2O4)>c(C2O42-) | |
| B. | pH=2的HF溶液与pH=12的氢氧化钠溶液等体积混合,所得溶液中:c(Na+)+c(OH-)>c(H+)+c(F-) | |
| C. | 向0.1mol/L的Na2S溶液中通入H2S至溶液呈中性(忽略体积变化),则溶液中:c(HS-)+2c(S2-)=0.2mol/L | |
| D. | 相同浓度的CH3COONa和NaClO的混合溶液中,各离子浓度的大小关系是:c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) |
