题目内容
19.一定条件下,在密闭容器中进行合成氨反应:N2(g)+3H2(g)?2NH3(g),当正、逆反应速率相等且不等于零时,下列说法不正确的是( )| A. | N2、H2、NH3在容器中共存 | B. | N2、H2、NH3的浓度不改变 | ||
| C. | 反应已达到化学平衡状态 | D. | N2、H2完全转化为NH3 |
分析 当正、逆反应速率相等且不等于零时,说明反应达到平衡状态,根据化学平衡状态的特征:逆、定、动、变、等来回答判断.
解答 解:A、可逆反应达到平衡状态时,各组分浓度不再改变,所以N2、H2、NH3在容器中共存,故A正确;
B、可逆反应达到平衡状态时,各组分浓度不再改变,故B正确;
C、当正、逆反应速率相等且不等于零时,说明反应达到平衡状态,故C正确;
D、可逆反应的反应物不可能完全转化,故D错误;
故选D.
点评 本题考查学生化学反应的可逆性以及平衡的特征知识,属于综合知识的考查,难度不大.

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
10.鉴别下列各组有机物所选试剂或方法不可行的是( )
| A. | 乙醇、甲苯、溴苯:水 | B. | 苯、环乙烯、环己烷:酸性KMnO4溶液 | ||
| C. | 乙醇、苯、四氯化碳:燃烧法 | D. | 乙醇、乙酸、乙酸乙酯:碳酸钠溶液 |
14.下列科学家对发现元素周期律贡献最大的是( )
| A. | 拉瓦锡 | B. | 道尔顿 | C. | 阿伏加德罗 | D. | 门捷列夫 |
4.NH5属于离子化合物,与水反应的化学方程式为:NH5+H2O=NH3.H2O+H2↑,有关NH5叙述正确的是( )
| A. | NH5的电子式: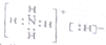 | |
| B. | NH5中N元素的化合价为+5价 | |
| C. | 1molNH5中含有5molN-H键 | |
| D. | 1molNH5与H2O完全反应,转移电子2mol |
11.下列说法正确的是( )
| A. | 单质分子中一定含有共价键 | |
| B. | 分子中只有共价键的化合物一定是共价化合物 | |
| C. | 活泼金属与活泼非金属化合时,一定形成离子键 | |
| D. | 只含非金属元素的化合物一定不是离子化合物 |
8.下列说法中,不正确的是( )
| A. | 石油裂解产物中有乙烯 | |
| B. | 天然气的主要成分是乙烯 | |
| C. | 芳香烃主要来自于煤干馏产生的煤焦油 | |
| D. | 汽油、煤油、柴油主要来自于石油的常压分馏 |

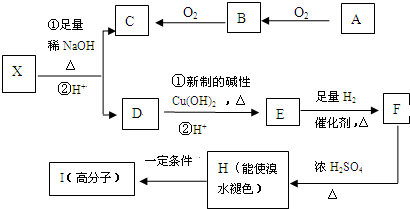
 ;
;