题目内容
4.已知:25℃时,Mg(OH)2的Ksp=5.61×10-12,MgF2的Ksp=7.42×10-11,下列判断正确的是( )| A. | 25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大 | |
| B. | 25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大 | |
| C. | 25℃时,Mg(OH)2固体在20mL 0.01mol/L的氨水中的Ksp比在20mL0.01mol/L NH4Cl溶液中的Ksp小 | |
| D. | 25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2不可能转化为MgF2 |
分析 根据氢氧化镁与氟化镁的化学式相似,由题中数据可知氢氧化镁的溶度积小,其饱和溶液中Mg2+浓度较小;氢氧化镁存在着微弱的电离,产生的氢氧根和氯化铵电离出来的铵根结合,产生一水合氨,使平衡正向移动,所以镁离子的浓度增加;Ksp只与温度有关;不管氢氧化镁的ksp有多小,只要加入的氟化钠溶液的浓度适合的话,使c(Mg2+)×c(F-)2>7.42×10-11,可以使氢氧化镁转化为氟化镁沉淀.
解答 解:A、因氢氧化镁溶度积小,由Ksp计算则其c(Mg2+)小,故A错误;
B、NH4+结合OH-使氢氧化镁溶解平衡正向移动,c(Mg2+)增大,故B正确;
C、Ksp不随浓度变化,只与温度有关,故C错误;
D、二者Ksp接近,加入NaF溶液后,Mg(OH)2和MgF2两种沉淀都会有,故D错误.
故选B.
点评 本题主要考查难溶电解质的溶解平衡和沉淀转化,注意比较两种物质的溶度积大小,特别提醒是的不同物质的溶度积比较应是在化学式相似的情况下具有可比性.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
12. 酸碱中和滴定是中学化学中重要的定量实验之一.
酸碱中和滴定是中学化学中重要的定量实验之一.
Ⅰ.某研究性学习小组准确进行了如下实验,称取1.00g不纯的苛性钠样品配成250ml溶液,取出10.00ml,用已知浓度为0.040mol•L-1的盐酸进行滴定(杂质不与盐酸反应).
根据要求回答下列问题:
(1)配制250mL 0.040mol•L-1的盐酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和250mL容量瓶.
(2)为测定该苛性钠溶液的准确浓度,几次滴定消耗盐酸的体积如下:
①计算苛性钠浓度时,哪次实验的数据不宜采用?答:3.(填实验序号)
②该苛性钠溶液的浓度为0.080 mol•L-1.
(3)若操作过程中未用盐酸润洗滴定管,对测定结果有怎样的影响?答:偏大(填“偏大”、“偏小”或“无影响”).
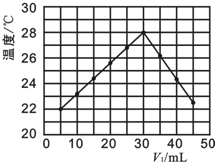
Ⅱ.在另一次实验中,研究性小组将V1 mL 1.0mol•L-1 HCl溶液和V2 mL 未知浓度的NaOH溶液均匀混合后,测量并记录溶液温度,实验结果如右图所示(实验中始终保持V1+V2=50mL).
(4)下列叙述中正确的是B
A.该实验的环境温度为22℃
B.当V1=40时,溶液中c(Na+)<c(Cl-)
C.NaOH溶液的浓度为1.0mol•L-1
D.保持其他条件不变,只将HCl改为CH3COOH
进行实验,也得到如图的实验结果.
 酸碱中和滴定是中学化学中重要的定量实验之一.
酸碱中和滴定是中学化学中重要的定量实验之一.Ⅰ.某研究性学习小组准确进行了如下实验,称取1.00g不纯的苛性钠样品配成250ml溶液,取出10.00ml,用已知浓度为0.040mol•L-1的盐酸进行滴定(杂质不与盐酸反应).
根据要求回答下列问题:
(1)配制250mL 0.040mol•L-1的盐酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和250mL容量瓶.
(2)为测定该苛性钠溶液的准确浓度,几次滴定消耗盐酸的体积如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗盐酸溶液的体积(mL) | 20.05 | 20.00 | 22.10 | 19.95 |
②该苛性钠溶液的浓度为0.080 mol•L-1.
(3)若操作过程中未用盐酸润洗滴定管,对测定结果有怎样的影响?答:偏大(填“偏大”、“偏小”或“无影响”).
Ⅱ.在另一次实验中,研究性小组将V1 mL 1.0mol•L-1 HCl溶液和V2 mL 未知浓度的NaOH溶液均匀混合后,测量并记录溶液温度,实验结果如右图所示(实验中始终保持V1+V2=50mL).
(4)下列叙述中正确的是B
A.该实验的环境温度为22℃
B.当V1=40时,溶液中c(Na+)<c(Cl-)
C.NaOH溶液的浓度为1.0mol•L-1
D.保持其他条件不变,只将HCl改为CH3COOH
进行实验,也得到如图的实验结果.
19.六氯丙烷(C3H2Cl6的同分异构体有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
9.工业炼铁是在高炉中进行的,高炉炼铁的主要反应是:
①2C(焦炭)+O2(空气)$\frac{\underline{\;高温\;}}{\;}$2CO②Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
该炼铁工艺中,对焦炭的实际使用量要远远高于按照化学方程式计算所需其主要原因是( )
①2C(焦炭)+O2(空气)$\frac{\underline{\;高温\;}}{\;}$2CO②Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
该炼铁工艺中,对焦炭的实际使用量要远远高于按照化学方程式计算所需其主要原因是( )
| A. | CO过量 | B. | CO与铁矿石接触不充分 | ||
| C. | 炼铁高炉的高度不够 | D. | CO与Fe2O3的反应有一定限度 |
16.化学与生产、生活、社会密切相关,下列说法不正确的是( )
| A. | 明矾[KAl(SO4)2•12H2O]溶于水会形成胶体,因此可用于自来水的杀菌消毒 | |
| B. | 小苏打是制作面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂 | |
| C. | 蛋白质、淀粉、油脂等都能在人体内水解并提供能量 | |
| D. | 纯净的二氧化硅是现代光学及光纤制品的基本原料 |
13.下列反应的离子方程式正确的是( )
| A. | 用氨水吸收过量的二氧化硫:NH3•H2O+SO2=NH4++HSO3- | |
| B. | 在澄清石灰水中通入少量二氧化碳:OH-+CO2=HCO3- | |
| C. | 向溴化亚铁中通入少量氯气:2Br-+Cl2=2Cl-+Br2 | |
| D. | 用氢氧化钠吸收多余的氯气:OH-+Cl2=2Cl-+HClO |
