题目内容
14.下列关于原电池说法正确的是( )| A. | 由Al、Mg、稀硫酸溶液组成的原电池,其负极反应式为:Al-3e-═Al3+ | |
| B. | 由Al、Mg、NaOH溶液组成的原电池,其负极反应式为:Al-3e-+3OH-═Al(OH)3↓ | |
| C. | 由Fe、Zn、NaCl溶液组成的原电池,其负极反应式为:Fe-2e-═Fe2+ | |
| D. | 由Al、Cu、浓硝酸溶液组成的原电池,其负极反应式为:Cu-2e-═Cu2+ |
分析 A.失电子的一极为负极,Mg比Al活泼,Mg失电子;
B.失电子的一极为负极,Al与氢氧化钠反应失电子,Mg不与氢氧化钠反应;
C.失电子的一极为负极,Zn比Fe活泼,Zn失电子;
D.失电子的一极为负极,Al遇到浓硝酸会钝化,Cu与浓硝酸反应失电子.
解答 解:A.失电子的一极为负极,由Al、Mg、稀硫酸组成的原电池,Mg比Al活泼,Mg失电子为负极,其负极反应式为:Mg-2e-═Mg2+,故A错误;
B.由Al、Mg、NaOH组成的原电池,Al做负极失电子生成AlO2-,其负极反应式为:2Al-6e-+4OH-═2AlO2-+2H2O故B错误;
C.Fe、Zn、NaCl溶液组成的原电池,金属锌Zn比Fe活泼,Zn失电子,发生吸氧腐蚀,负极反应为Zn-2e-═Zn2+,故C错误;
D.由Al、Cu、浓硝酸组成的原电池,Al遇到浓硝酸会钝化,Cu与浓硝酸反应失电子,Cu作负极,其负极反应式为:Cu-2e-═Cu2+,故D正确;
故选D.
点评 本题考查原电池知识,侧重于原电池的组成、电极以及工作原理的考查,题目难度不大,注意相关基础知识的理解.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
4.下列说法中正确的是( )
| A. | 纯净物一定由分子组成 | |
| B. | 由同种分子构成的物质一定是纯净物 | |
| C. | 混合物一定是由两种以上元素构成的 | |
| D. | 含有氧元素的化合物都是氧化物 |
9.将铜片、铁片平行插在稀硫酸中,用导线连接起来并接入电流表,下列判断正确的是( )
| A. | 铜片在溶解,铁片上有无色气体生成 | |
| B. | 电流表指针没有偏转 | |
| C. | 电子从铁片流出经过导线流向铜片 | |
| D. | 电池总反应为Cu+2H+═H2+Cu2+ |
19.下列实验装置或操作正确的是( )
| A. | 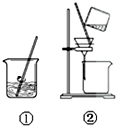 除去附着在铁屑表面的铝 | B. | 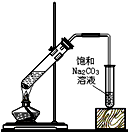 实验室制取乙酸乙酯 | ||
| C. | 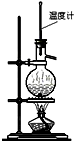 实验室制乙烯 | D. |  分离酒精和水 |
6.下列说法一定正确的是( )
| A. | 酸性物质与酸性物质、碱性物质与碱性物质不能反应 | |
| B. | 溶液中某离子浓度减小发生了化学反应 | |
| C. | 含同一元素的不同化合物,该元素的化合价越高,其氧化性越强 | |
| D. | 多个电解池串联,通过每个电极电子的物质的量相等 |
3.下列说法正确的是( )
| A. | 需要加热方能发生的反应一定是吸热反应 | |
| B. | 放热的反应在常温下一定很容易发生 | |
| C. | 吸热反应在一定条件下也能发生 | |
| D. | H2(g)+$\frac{1}{2}$O2(g)=H2O(g);△H=-235.8 kJ/mol 则氢气的燃烧热为235.8KJ/mol |
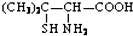 ,请写出青霉氨基酸可能具有的一种化学性质能与碱发生中和反应.
,请写出青霉氨基酸可能具有的一种化学性质能与碱发生中和反应.