题目内容
【题目】碱式碳酸钠铝[NaaAlb(OH)c(CO3)d]可用作阻燃剂、抗酸剂等。其制备方法是:控制温度、pH,向NaHCO3稀溶液中加入Al(OH)3,并搅拌,充分反应后过滤、洗涤、干燥,得碱式碳酸钠铝。
(1)碱式碳酸钠铝[NaaAlb(OH)c(CO3)d]中a、b、c、d之间的关系为________。
(2)碱式碳酸钠铝作为阻燃剂的可能原因:①在分解过程中大量吸热;②本身及产物无毒且不可燃;③________________________。
(3)若pH过高,则对产品的影响是________________________。
(4)为确定碱式碳酸钠铝的组成,进行如下实验:
①准确称取2.880 g样品用足量稀硝酸溶解,得到CO2 0.448 L(已换算成标准状况下),并测得溶液中含有0.02 mol Al3+。
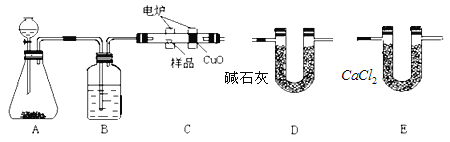
②加热至340 ℃以上时样品迅速分解,得到金属氧化物、CO2和H2O。当样品分解完全时,样品的固体残留率(固体样品的剩余质量/固体样品的起始质量×100%)为56.9%,根据以上实验数据确定碱式碳酸钠铝的组成(写出计算过程)。
【答案】(1)a+3b=c+2d(2分)
(2)产生阻燃性气体CO2、H2O(2分)
(3)pH过高会使碱式碳酸钠铝转化为NaAlO2(2分)
(4)NaAl(OH)2CO3 (6分)
n(CO2)=![]() =0.02 mol (1分)
=0.02 mol (1分)
n(H2O)=![]() =0.02 mol(1分)
=0.02 mol(1分)
b∶c∶d=1∶2∶1,根据电荷守恒,a∶b∶c∶d=1∶1∶2∶1(2分)
所以,碱式碳酸铝的化学组成为NaAl(OH)2CO3(2分)
【解析】
试题分析:(1)碱式碳酸钠铝[NaaAlb(OH)c(CO3)d]中,化合价代数和为0,所以a+3b-c-2d=0,则a+3b=c+2d。
故答案为:a+3b=c+2d;
(2)碱式碳酸钠铝作为阻燃剂的可能原因:①在分解过程中大量吸热;②本身及产物无毒且不可燃;③同产生不支持燃烧的二氧化碳和水。
故答案为:产生阻燃性气体CO2、H2O;
(3)pH过高,碱性强不生成氢氧化铝,而产生偏铝酸盐,所以pH过高,则对产品的影响是会使碱式碳酸钠铝转化为NaAlO2。
故答案为:pH过高会使碱式碳酸钠铝转化为NaAlO2;
(4)因为:n(CO2)=![]() =0.02 mol,
=0.02 mol,
n(H2O)=![]() =0.02 mol,
=0.02 mol,
而测得溶液中含有0.02molAl3+,所以b:c:d=1:2:1,根据电荷守恒a+0.02×3=0.02×2+0.02×2,所以a=0.02mol,所以a:b:c:d=1:1:2:1,所以,碱式碳酸铝的化学组成为NaAl(OH)2CO3。
故答案为:NaAl(OH)2CO3 (6分)
n(CO2)=![]() =0.02 mol (1分)
=0.02 mol (1分)
n(H2O)=![]() =0.02 mol(1分)
=0.02 mol(1分)
b∶c∶d=1∶2∶1,根据电荷守恒,a∶b∶c∶d=1∶1∶2∶1(2分)
所以,碱式碳酸铝的化学组成为NaAl(OH)2CO3(2分)