题目内容
19. 某密闭容器中发生如下反应:2X(g)+Y(g)?Z(g);△H<0 如图表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5 时刻外界条件有所改变,但都没有改变各物质的用量.则下列说法中不正确的是( )
某密闭容器中发生如下反应:2X(g)+Y(g)?Z(g);△H<0 如图表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5 时刻外界条件有所改变,但都没有改变各物质的用量.则下列说法中不正确的是( )| A. | t3 时降低了压强 | |
| B. | t5 时提高了温度 | |
| C. | t1-t2 时该反应的平衡常数小于 t6时反应的平衡常数 | |
| D. | t6 时刻后反应物的转化率最低 |
分析 由图可知,t2时刻,改变条件,正、逆反应速率同等程度增大,平衡不移动.该反应正反应是气体体积减小的反应,增大压强平衡向正反应移动,不可能是改变压强,故改变条件为使用催化剂;
t3时刻,改变体积,正、逆反应速率降低,且正反应速率降低更多,平衡向逆反应移动.该反应正反应是放热反应,温度降低,平衡向正反应移动,故不可能为降低温度,该反应正反应是气体体积减小的反应,减小压强平衡向逆反应移动,故改变条件为减小压强;
t5时刻,改变条件,正、逆反应速率都增大,且逆反应速率增大更多,平衡向逆反应移动.该反应正反应是气体体积减小的反应,增大压强平衡向正反应移动,不可能是改变压强,该反应正反应是放热反应,升高温度,平衡向逆反应移动,故改变条件为升高温度.
解答 解:由图可知,t2时刻,改变条件,正、逆反应速率同等程度增大,平衡不移动.该反应正反应是气体体积减小的反应,增大压强平衡向正反应移动,不可能是改变压强,故改变条件为使用催化剂;
t3时刻,改变体积,正、逆反应速率降低,且正反应速率降低更多,平衡向逆反应移动.该反应正反应是放热反应,温度降低,平衡向正反应移动,故不可能为降低温度,该反应正反应是气体体积减小的反应,减小压强平衡向逆反应移动,故改变条件为减小压强;
t5时刻,改变条件,正、逆反应速率都增大,且逆反应速率增大更多,平衡向逆反应移动.该反应正反应是气体体积减小的反应,增大压强平衡向正反应移动,不可能是改变压强,该反应正反应是放热反应,升高温度,平衡向逆反应移动,故改变条件为升高温度;
A、t3 时减小了压强,故A正确;
B、t5改变条件为升高温度,故B正确;
C、正反应为放热反应,t5改变条件为升高温度,平衡常数减小,t1-t2 时该反应的平衡常数大于t6时反应的平衡常数,故C错误;
D、由上述分析可知,t2时刻,使用催化剂,平衡不移动,X的转化率不变,t3时刻,减小压强,平衡向逆反应移动,X的转化率降低,t5时刻,升高温度,平衡向逆反应移动,X的转化率继续降低,故在t6时刻,X的转化率最低,故D正确;
故选C.
点评 本题考查反应速率与时间图象、影响反应速率与化学平衡移动的因素,难度中等,注意根据正、逆速率判断平衡移动方法.

| A. | 含有2NA个氦原子的氦气在标准状况下的体积约为22.4L | |
| B. | 25℃,1.01×105 Pa,64g SO2中含有的O原子数为2NA | |
| C. | 在常温常压下,22.4L Cl2含有的分子数为NA | |
| D. | 标准状况下,11.2LCH3CH2OH(酒精)含有的分子数为0.5NA |
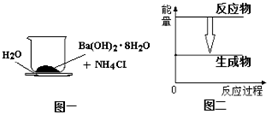 用玻璃棒迅速搅拌如图所示装置内(小烧杯与玻璃片之间有一薄层水)的固体混合物.稍后手拿起烧杯时发现玻璃片与烧杯粘结在一起.下列有关该反应的说法中正确的是( )
用玻璃棒迅速搅拌如图所示装置内(小烧杯与玻璃片之间有一薄层水)的固体混合物.稍后手拿起烧杯时发现玻璃片与烧杯粘结在一起.下列有关该反应的说法中正确的是( )| A. | 反应中有化学能转化为热能 | B. | 反应中的能量关系如图二 | ||
| C. | 是吸热反应 | D. | 化学键的总键能:反应物<生成物 |
| A. | 1.25 | B. | 2 | C. | 2.25 | D. | 3.2 |
| A. | 酚酞试剂 | B. | BaCl2溶液 | C. | 石蕊试剂 | D. | Na2CO3溶液 |
| A. | 铜片上发生了还原反应 | |
| B. | 电子通过导线由铜片流向锌片 | |
| C. | 正极有O2逸出 | |
| D. | 正极附近的SO42-离子浓度逐渐增大 |