题目内容
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.![]() =1012的溶液中:Fe2+、Mg2+、NO
=1012的溶液中:Fe2+、Mg2+、NO![]() 、Cl-
、Cl-
B.澄清透明的溶液中:H+、Cu2+、SO![]() 、NO
、NO![]()
C.0.1mol/L的NaHCO3溶液中:Fe3+、K+、Cl-、SO![]()
D.由水电离产生的c(H+)=1×10-12mol/L的溶液中:K+、Al3+、Cl-、SO![]()
【答案】B
【解析】
A.![]() =1012的溶液中显酸性,酸性溶液中NO3-会将Fe2+氧化而不能大量共存,故A不符合题意;
=1012的溶液中显酸性,酸性溶液中NO3-会将Fe2+氧化而不能大量共存,故A不符合题意;
B.四种离子相互之间不反应,可以在澄清透明的溶液中大量共存,故B符合题意;
C.Fe3+可以与HCO3-相互促进水解,生成Fe(OH)3和CO2,不能大量共存,故C不符合题意;
D.水电离产生的c(H+)=1×10-12mol/L的溶液中水的电离受到抑制,可能是酸溶液也可能是碱溶液,碱溶液中Al3+不能大量存在,故D不符合题意;
答案为B。

【题目】过氧化氢是重要的化工产品,广泛应用于化学合成、医疗消毒等领域。
(1)过氧化氢的电子式为_____________。
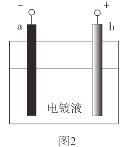
(2)工业上电解硫酸氢盐溶液得到过二硫酸盐(![]() ),过二硫酸盐水解生成H2O2溶液和硫酸氢盐,生成的硫酸氢盐可以循环使用。电解硫酸氢盐溶液时阳极的电极反应式为_______。写出过二硫酸盐水解的离子方程式________。
),过二硫酸盐水解生成H2O2溶液和硫酸氢盐,生成的硫酸氢盐可以循环使用。电解硫酸氢盐溶液时阳极的电极反应式为_______。写出过二硫酸盐水解的离子方程式________。
(3)298K时,实验测得反应![]() 在不同浓度时的化学反应速率如表:
在不同浓度时的化学反应速率如表:
实验编号 | 1 | 2 | 3 | 4 | |
c(HI) /mol﹒L-1 | 0.100 | 0.200 | 0.300 | 00.100 | 0.100 |
c(H2O2)/mol﹒L-1 | 0.100 | 0.100 | 0.100 | 0.200 | 0.300 |
v//mol﹒L-1﹒s-1 | 0.007 60 | 0.015 3 | 0.022 7 | 0.015 1 | 0.022 8 |
已知速率方程为![]() ,其中k为速率常数。
,其中k为速率常数。
根据表中数据判断:a=_______,b=________。
(4)“大象的牙膏”实验是将浓缩的过氧化氢与肥皂液混合,再滴加少量碘化钾溶液,即可观察到泡沫状物质像喷泉一样喷涌而出。反应中H2O2的分解机理为:
![]() 慢
慢
![]() 快
快
此反应过程中无催化剂和有催化剂的能量变化关系图像如图所示:

则表示慢反应的曲线是__________(填“a”或“b”)。
1mol H2O2分解放出热量98 kJ,则H2O2分解的热化学方程式为_________________。
(5)某科研团队研究![]() 体系(其中
体系(其中![]() )氧化苯乙烯制取苯甲醛,反应的副产物主要为苯甲酸和环氧苯乙烷。一定条件下,测得一定时间内温度对氧化反应的影响如图:
)氧化苯乙烯制取苯甲醛,反应的副产物主要为苯甲酸和环氧苯乙烷。一定条件下,测得一定时间内温度对氧化反应的影响如图:

注:■苯乙烯转化率 ●苯甲醛选择性
①80℃时苯乙烯的转化率有所降低,其原因可能是_______。
②结合苯乙烯的转化率,要获得较高的苯甲醛产率,应该选择的温度为_______。
【题目】25℃时,三种酸的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.8×10-5 | K14.3×10-7 K25.6×10-11 | 3.0×10-8 |
回答下列问题:
(1)一般情况下,当温度升高时,Ka__(填“增大”、“减小”或“不变”)。
(2)下列四种离子结合质子能力由大到小的顺序是__(填序号);
a.CO![]() b.ClO-c.CH3COO-d.HCO
b.ClO-c.CH3COO-d.HCO![]()
(3)下列反应不能发生的是__(填序号)
a.CO![]() +CH3COOH=CH3COO-+CO2↑+H2O
+CH3COOH=CH3COO-+CO2↑+H2O
b.ClO-+CH3COOH=CH3COO-+HClO
c.CO![]() +2HClO=CO2↑+H2O+2ClO-
+2HClO=CO2↑+H2O+2ClO-
d.2ClO-+CO2+H2O=CO![]() +2HClO
+2HClO
(4)体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。

则HX的电离平衡常数__(填“大于”、“等于”或“小于”,下同)醋酸的电离平衡常数;稀释后,HX溶液中水电离出来的c(H+)__醋酸溶液中水电离出来的c(H+),理由是___。