题目内容
【题目】甲醇是一种重要的试剂,氢气和二氧化碳在一定条件下可合成甲醇:CO2(g)+3H2 (g) ![]() CH3 OH(g)+H2O(g),在密闭容器中充入3mol氢气和1mol二氧化碳,测得混合气体中甲醇的体积分数与温度的关系如图A所示:
CH3 OH(g)+H2O(g),在密闭容器中充入3mol氢气和1mol二氧化碳,测得混合气体中甲醇的体积分数与温度的关系如图A所示:

试回答下列问题:
(1)该反应是______(填“放热”或“吸热”)反应。该反应平衡常数的表达式是:______,为了降低合成甲醇的成本可采用的措施是______(任意写一条合理的建议)
(2)解释0~T0内,甲醇的体积分数变化趋势:______。
(3)氢气在Q点的转化率______(填“大于”、“小于”或“等于”,下同)氢气在W点的转化率______;其它条件相同,甲醇在Q点的正反应速率______甲醇在M点的正反应速率。
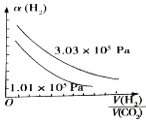
(4)图B表示氢气转化率α(H2)与投料比![]() 的关系,请在图B中画出两条变化曲线并标出曲线对应的条件,两条曲线对应的条件分别为:一条曲线对应的压强是1.01×105Pa;另一条曲线对应的压强是3.03×105Pa(其它条件相同)
的关系,请在图B中画出两条变化曲线并标出曲线对应的条件,两条曲线对应的条件分别为:一条曲线对应的压强是1.01×105Pa;另一条曲线对应的压强是3.03×105Pa(其它条件相同)
【答案】
(1)放热;![]() ;增加CO2的充入量
;增加CO2的充入量
(2)温度低于T0时,反应未达到平衡,反应正向进行,使甲醇的体积分数逐渐增大
(3)小于;小于
(4) ;
;
【解析】
试题分析:(1)T0时,升高温度,甲醇的体积分数减小,平衡逆向移动,正反应为放热反应;该反应平衡常数的表达式为![]() ,为了降低合成甲醇的成本,应该尽可能的使平衡向右移动,可采用的措施有增加CO2的充入量等,故答案为:放热;
,为了降低合成甲醇的成本,应该尽可能的使平衡向右移动,可采用的措施有增加CO2的充入量等,故答案为:放热;![]() ;增加CO2的充入量;
;增加CO2的充入量;
(2)温度低于T0时,反应未达到平衡,反应正向进行,使甲醇的体积分数逐渐增大,故答案为:温度低于T0时,反应未达到平衡,反应正向进行,使甲醇的体积分数逐渐增大;
(3)温度低于T0时,反应未达到平衡,反应正向进行,氢气在Q点的转化率小于平衡时的转化率,W点打到平衡,因此氢气在Q点的转化率小于W点的转化率;平衡之前,甲醇的正反应速率逐渐增大,甲醇在Q点的正反应速率小于W点的反应速率,升高温度,反应速率增大,甲醇在M点的正反应速率大于W点,因此甲醇在Q点的正反应速率小于在M点的正反应速率,故答案为:小于;小于;
(4)根据方程式,增大压强,平衡正向移动,氢气转化率α(H2)增大,增大投料比![]() ,氢气转化率α(H2)减小,因此图像为
,氢气转化率α(H2)减小,因此图像为 ,故答案为:
,故答案为: 。
。

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案【题目】水煤气 (主要成分CO、H2 ) 是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C (s) + H2O(g)![]() CO (g) +H2 (g);△H =+131.3kJmol-1
CO (g) +H2 (g);△H =+131.3kJmol-1
(1)某温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
容器编号 | c(H2O)/mol·L-1 | c(CO)/mol·L-1 | c(H2)/mol·L-1 | V正、V逆比较 |
I | 0.06 | 0.60 | 0.10 | V正=V逆 |
II | 0.06 | 0.50 | 0.40 | (_________) |
III | 0.12 | 0.40 | 0.80 | V正<V逆 |
IV | 0.12 | 0.30 | _________ | V正=V逆 |
(2)另有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0mol炭和 1.0mo l水蒸气 (H216O),发生上述反应,达到平衡时,容器的体积变为原来的1.25 倍。平衡时水蒸气的转化率为___________;向该容器中补充 a mol 炭,水蒸气的转化率将____________(填 “增大”、“减小”、“不变”),再补充 a mol 水蒸气 (H218O), 最终容器中C16O和C18O 的物质的量之比为_____________。



