题目内容
19.在加入铝粉能放出氢气的溶液中,下列各组离子可能大量共存的是( )| A. | NH4+、NO3-、CO32-、Na+ | B. | Na+、Ba2+、HCO3-、AlO2- | ||
| C. | NO3-、K+、AlO2-、OH-? | D. | NO3-、Mg2+、K+、CH3COO-? |
分析 加入铝粉能放出氢气的溶液,为非氧化性酸或强碱溶液,根据离子之间不能结合生成沉淀、气体、水、弱电解质等,则离子大量共存,以此来解答.
解答 解:加入铝粉能放出氢气的溶液,为非氧化性酸或强碱溶液,
A.酸溶液中不能大量存在CO32-,碱溶液中不能大量存在NH4+,故A不选;
B.AlO2-促进HCO3-的电离,且酸溶液中不能大量存在HCO3-、AlO2-,碱溶液中Ba2+、HCO3-结合生成沉淀,故B不选;
C.碱溶液中该组离子之间不反应,可大量共存,故C选;
D.碱溶液中不能大量存在Mg2+,酸溶液中不能大量存在CH3COO-,且Al、NO3-、H+发生氧化还原反应不生成氢气,故D不选;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重氧化还原反应、复分解反应的离子共存考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.在冶金工业上,均不能用化学还原法制得的一组金属是( )
| A. | K、Na、Al | B. | Na、K、Zn、Fe | C. | Zn、Fe、Cu、Ag | D. | Mg、Al、Zn、Fe |
7.有一种合成维生素的结构简式为 ,对该合成维生素的叙述正确的是( )
,对该合成维生素的叙述正确的是( )
 ,对该合成维生素的叙述正确的是( )
,对该合成维生素的叙述正确的是( )| A. | 该合成维生素有三个苯环 | |
| B. | 该合成维生素1 mol最多能中和5 mol氢氧化钠 | |
| C. | 该合成维生素1 mol最多能和含6 mol单质溴的溴水反应 | |
| D. | 该合成维生素可用有机溶剂萃取 |
14.${\;}_{6}^{13}$C-NMR用于含碳化合物的结构分析.${\;}_{6}^{13}$C表示的碳原子( )
| A. | 核外有13个电子 | |
| B. | 核内有6个质子,核外有7个电子 | |
| C. | 质量数为13,原子序数为6,核内有7个中子 | |
| D. | 质量数为13,原子序数为6,核内有7个质子 |
11.下面不能由单质直接化合而得到的化合物是( )
| A. | FeS | B. | Al2S3 | C. | FeCl2 | D. | Fe3O4 |
9.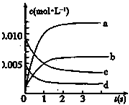 在2L密闭容器内,800℃时反应:2XY (g)+Y2(g)?2XY2(g)体系中,n(XY)随时间的变化如表:
在2L密闭容器内,800℃时反应:2XY (g)+Y2(g)?2XY2(g)体系中,n(XY)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K=$\frac{c(XY{\;}_{2}){\;}^{2}}{c(XY){\;}^{2}c(Y{\;}_{2})}$.
(2)如图中表示XY2的变化的曲线是b.用Y2表示从0~2s内该反应的平均速率v=0.0015mol•L-1•S-1.
(3)能说明该反应已达到平衡状态的是B.
A.v(XY2)=2v(Y2)
B.容器内压强保持不变
C.XY、Y2、XY2的浓度之比为2:1:2
D.容器内密度保持不变.
 在2L密闭容器内,800℃时反应:2XY (g)+Y2(g)?2XY2(g)体系中,n(XY)随时间的变化如表:
在2L密闭容器内,800℃时反应:2XY (g)+Y2(g)?2XY2(g)体系中,n(XY)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(XY)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图中表示XY2的变化的曲线是b.用Y2表示从0~2s内该反应的平均速率v=0.0015mol•L-1•S-1.
(3)能说明该反应已达到平衡状态的是B.
A.v(XY2)=2v(Y2)
B.容器内压强保持不变
C.XY、Y2、XY2的浓度之比为2:1:2
D.容器内密度保持不变.
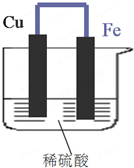 如图所示,将铁、铜通过导线相连,置于稀硫酸中.
如图所示,将铁、铜通过导线相连,置于稀硫酸中.