��Ŀ����
����Ŀ��ʵ��������NaOH ��������1.0mol/L��NaOH��Һ240mL��
��1��������Һʱ��һ����Է�Ϊ���¼������裺
�ٳ��� �ڼ��� ���ܽ� �ܵ�תҡ�� ��ת�� ��ϴ�� �߶��� ����ȴ
��ʵ������õ�����������ƽ��ҩ�ס����������ձ�����ͷ�ιܡ�___��
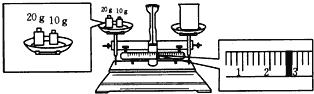
��2��ijͬѧ������һ������NaOH���壬������������ƽ�����ձ�����������ƽƽ����״̬��ͼ��ʾ���ձ���ʵ������Ϊ___g��Ҫ��ɱ�ʵ���ͬѧӦ�Ƴ�___gNaOH��
��3�������ƹ����У���������������ȷ�ģ����в���������Ũ��ƫ�ߵ���___��
��û��ϴ���ձ��Ͳ����� ��ת����Һʱ������������������ƿ����
������ƿ�����������������ˮ �ܶ���ʱ���ӿ̶���
���𰸡�250mL����ƿ 27.4 10.0g ��
��������
��1�����ݲ�����Ҫ��250mL����ƿ��
��2����ƽ��ƽ��ԭ������m��=m��+����������ѡȡ����ƿ���ݻ������������Ƶ�������
��3������![]() ����ʵ����
����ʵ����
��1�����ݲ�����Ҫ��250mL����ƿ�����Ա�ʵ������õ�����������ƽ��ҩ�ס����������ձ�����ͷ�ιܡ�250mL����ƿ��
��2��m��=m��+�Σ���߷���30g�����룬���������2.6g������m�ձ�=30g-2.6g=27.4g��ѡȡ����ƿ���ݻ���250mL��m(NaOH)=cVM=1.0mol/L��0.25L��40g/mol=10.0g��
��3����û��ϴ���ձ��Ͳ����������ʵ����ʵ���ƫС��������ҺŨ��ƫ�ͣ��ʲ�ѡ����
��ת����Һʱ������������������ƿ���棬���ʵ����ʵ���ƫС��������ҺŨ��ƫ�ͣ��ʲ�ѡ����
���������ˮ����������ƿ�����������������ˮ��������ҺŨ����Ӱ�죬�ʲ�ѡ��
������ʱ���ӿ̶��ߣ���Һ���ƫС��������ҺŨ��ƫ�ߣ���ѡ����

