题目内容
【题目】现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出金属元素A的原子结构示意图:_______________。
(2)写出下列反应的离子方程式:反应③_____________
反应⑤________________
(3)检验物质G中阳离子的操作方法_________________________________________。
(4)保存物质F的溶液时,要加入____________,目的是______________。
【答案】 Na 2Al+2OH-+2H2O=2AlO2-+3H2↑ 2Fe2++Cl2=2Fe3++2Cl- 取物质G少量于试管中,向其中滴加少量的KSCN溶液,溶液变成血红色,证明物质G中有Fe3+离子 铁屑 防止Fe2+氧化为Fe3+
2Al+2OH-+2H2O=2AlO2-+3H2↑ 2Fe2++Cl2=2Fe3++2Cl- 取物质G少量于试管中,向其中滴加少量的KSCN溶液,溶液变成血红色,证明物质G中有Fe3+离子 铁屑 防止Fe2+氧化为Fe3+
【解析】金属单质A的焰色反应为黄色,则A为金属Na;反应①为Na与水反应生成NaOH和H2,则气体甲为H2,D为NaOH;黄绿色气体乙为Cl2,则丙为HCl,E为盐酸;反应③为金属B与NaOH反应生成H2,能与碱反应生成H2的金属为Al,即B为Al;反应⑥NaOH与物质G反应生成红褐色沉淀,红褐色沉淀为Fe(OH)3,则物质G中含有Fe3+;金属C与盐酸反应生成F,F与氯气反应生成物质G,则金属C为Fe,F为FeCl2,氯化亚铁与氯气反应生成G为FeCl3。
(1)A为Na,Na元素为11号原子,则原子结构示意图为: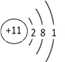 ;
;
(2)反应③为Al与NaOH溶液的反应,离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;反应⑤为FeCl2与Cl2反应生成FeCl3,离子方程式为:2Fe2++Cl2=2Fe3++2Cl-。
(3)G物质为FeCl3,Fe3+的检验方法为:取少量G溶液于试管中,向其中滴加几滴KSCN溶液,溶液变成血红色,证明物质G中有Fe3+离子。
(4)F物质为FeCl2,Fe2+容易被氧化,配制和保存FeCl2时,加入少量铁屑,Fe可以与FeCl3反应:Fe+2FeCl3=3FeCl2,即加入铁屑可以防止Fe2+被氧化为Fe3+。