题目内容
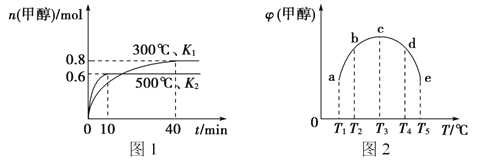
【题目】CO和H2在一定条件下合成甲醇的反应为;CO(g)+2H2(g)![]() CH3OH(g) △H1。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控制温度,进行实验,测得相关数据如图(图1:温度分别为300℃ 、500℃的密闭容器中,甲醇的物质的量:图2:温度分别为Tl~T5的密闭容器中,反应均进行到5min时甲醇的体积分数)。下列叙述正确的是
CH3OH(g) △H1。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控制温度,进行实验,测得相关数据如图(图1:温度分别为300℃ 、500℃的密闭容器中,甲醇的物质的量:图2:温度分别为Tl~T5的密闭容器中,反应均进行到5min时甲醇的体积分数)。下列叙述正确的是
A. 该反应的△H1>0,且K1>K2
B. 将容器c中的平衡状态转变到容器d中的平衡状态,可采取的措施有升温或加压
C. 300℃时,向平衡后的容器中再充入0.8molCO, 0.6molH2,0.2molCH3OH,平衡正向移动
D. 500℃时,向平衡后的容器中再充入1molCH3OH,重新平衡后,H2浓度和百分含量均增大
【答案】C
【解析】A、由图1可知,升高温度,甲醇减少,平衡逆向移动,正向放热,△H1<0,且K1>K2,故A错误;B、正反应放热,反应后体积减小,从c到d,甲醇减少,平衡逆向移动,故可采取的措施有升温或减压,故B错误;C、先算平衡常数,平衡时甲醇的物质的量为0.8mol 代入平衡常数计算式
代入平衡常数计算式![]() ,300℃时,向平衡后的容器中再充入0.8molCO, 0.6molH2,0.2molCH3OH,浓度商Qc=
,300℃时,向平衡后的容器中再充入0.8molCO, 0.6molH2,0.2molCH3OH,浓度商Qc= ,平衡正向移动,故C正确;D、500℃时,向平衡后的容器中再充入1molCH3OH,相当于增大压强,平衡正向移动,重新平衡后,H2浓度增大,但百分含量均减小,故D错误;故选C。
,平衡正向移动,故C正确;D、500℃时,向平衡后的容器中再充入1molCH3OH,相当于增大压强,平衡正向移动,重新平衡后,H2浓度增大,但百分含量均减小,故D错误;故选C。

练习册系列答案
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案
相关题目