题目内容
【题目】下列图示与对应的叙述相符的是

A. 若图1表示0.2mo1MgCl2·6H2O在空气中充分加热时固体质量随时间的变化,则a为19.0
B. 若图2表示常温下用0.1000mo1/L NaOH溶液滴定25.00mL CH3COOH溶液的滴定曲线,则c(CH3COOH)=0.1000mo1/L
C. 若图3表示常温下稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则常温下,NaA溶液的pH小于同浓度的NaB溶液的pH
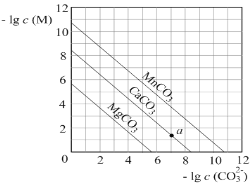
D. 若图4表示恒温恒容条件下,反应2NO2(g)![]() N2O4(g)中,各物质的浓度与其消耗速率之间的关系,则b点对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,则b点对应的状态为化学平衡状态
【答案】C
【解析】
A.MgCl2为强酸弱碱盐,其结晶水合物在空气中加热最终转化为氧化镁,根据Mg元素守恒,0.2mo1MgCl2·6H2O 分解产生0.2molMgO,其质量m(MgO)=0.2mol×40g/mol=8.0g,最终生成质量应为8.0g,A错误;
B.0.1000 mol/L的NaOH溶液滴定25.00 mLCH3COOH,当溶液pH=7时,溶液中c(H+)=c(OH-),若酸碱恰好中和,溶液为醋酸钠溶液,由于醋酸是一元弱酸,醋酸钠是强碱弱酸盐,在溶液中CH3COO-水解使溶液呈碱性,实际上溶液为中性,说明此时溶液中应同时存在醋酸和醋酸钠,由于醋酸并未完全反应,所以无法计算醋酸的浓度,B错误;
C.常温下,稀释HA、HB两种酸的稀溶液,溶液酸性越强,溶液稀释时,其pH变化幅度越大,根据图象可知,酸性:HA>HB。酸的酸性越强,其对应的强碱盐的碱性就越弱,则NaA的碱性比NaB弱,则同浓度的两溶液的pH:NaA<NaB,C正确;
D.恒温恒容条件下,发生可逆反应:2NO2(g)![]() N2O4(g),根据图象,b点表示消耗N2O4的速率等于NO2的消耗速率,表明逆反应速率大于正反应速率,反应逆向进行,不是化学平衡状态,D错误;
N2O4(g),根据图象,b点表示消耗N2O4的速率等于NO2的消耗速率,表明逆反应速率大于正反应速率,反应逆向进行,不是化学平衡状态,D错误;
故合理选项是C。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案