题目内容
14.向淀粉溶液中加入少量的稀硫酸并加热,使淀粉发生水解,为测定其水解程度,所需的试剂是( )①NaOH溶液 ②银氨溶液 ③新制Cu(OH)2悬浊液 ④碘水 ⑤BaCl2溶液.
| A. | ④ | B. | ③⑤ | C. | ②④ | D. | ①③④ |
分析 淀粉在酸性条件下水解生成葡萄糖,检验葡萄糖用银氨溶液或新制Cu(OH)2碱性悬浊液,而醛基的银镜反应和与新制氢氧化铜悬浊液的反应均在碱性条件下进行,检验淀粉用碘水.据此分析.
解答 解:淀粉在酸性条件下水解生成葡萄糖,而醛基的银镜反应和与新制氢氧化铜悬浊液的反应均在碱性条件下进行,故检验水解有无葡萄糖生成时,应先用NaOH溶液调节溶液至碱性,然后用银氨溶液或新制Cu(OH)2碱性悬浊液检验,最后用碘水检验淀粉是否完全水解,故选D.
点评 本题考查淀粉水解程度的检验,题目难度不大,醛基的银镜反应和与新制氢氧化铜悬浊液的反应均在碱性条件下进行,注意反应环境对反应的影响.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.实验室配制500mL0.1mol•L -1Na2CO3溶液.下列说法正确的是( )
| A. | 若定容时,加水越过刻度线,则所配得溶液的浓度偏高 | |
| B. | 若忘记将洗涤液加入容量瓶,则所配得溶液的浓度偏低 | |
| C. | 若定容后摇匀液面低于刻度线,再加水至刻度线,所得溶液浓度为0.1mol•L -1 | |
| D. | 若定容时俯视刻度线,则所配得溶液浓度偏高 |
5.下列各组离子一定能大量共存的是( )
| A. | 在透明溶液中:NH4+、Fe2+、SO42-、Cl- | |
| B. | 在强酸性溶液中:K+、Fe2+、Cl-、NO3- | |
| C. | 在强碱性溶液中:Na+、K+、Cl-、NH4+ | |
| D. | 与铝作用产生H2的溶液:Mg2+、K+、Cl-、SO42- |
2.下列物质的水溶液中,除水分子外,还存在其他分子的是( )
| A. | HCl | B. | CH3COOH | C. | KNO3 | D. | NaOH |
19.对人体中的所需元素,下列四位同学归纳整理完全正确的一组是( )
| A. | 小芳认为,人体缺乏下列元素,会得不同疾病.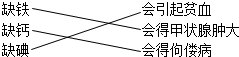 | |
| B. | 小槐搜集资料发现,生活中人们常通过下列途径来补充人体必需的营养元素.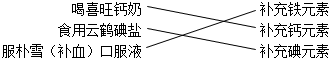 | |
| C. | 小蓉为下列元素各设计了一句广告词来反映其对人体的重要作用. | |
| D. | 小红搜集资料发现,长期或大量摄入铝元素对人体的大脑和神经系统将造成损害,他提出下列建议: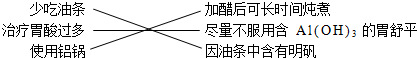 |
2.含氧酸的元数等于羟基氢的个数,氢氧化钠只能中和连在氧上的羟基氢,磷元素有多种含氧酸,如次磷酸(H3PO2)、亚磷酸(H3P03)、磷酸等,它们分别为一元、二 元、三元弱酸或中强酸.
(1)其中次磷酸钠常用来给腈纶织物进行化学镀,某种碱性化学镀铜试剂的配方有次磷酸钠和硫酸铜,产物中有亚磷酸钠的正盐,请写出相关离子方程式:H2PO2-+Cu2++3OH-=Cu↓+HPO32-+2H2O.
(2)亚磷酸可以由三氯化磷水解得到,也可以由电解亚磷酸钠来制备,如图1是用一个六室电渗析槽制备亚磷酸.其中阳极室和产品室之间的阳离子膜主要目的是防止:2H3PO3+O2=2H3PO4(只要求写出化学方程式),这种方法的产品除了有亚磷酸,还有:氧气、氢气、氢氧化钠,如果去掉右边两个阳离子膜(没有了右边的缓冲室),带来的不利后果是(填序号):B.
A、氢氧化钠与原料Na2HP03会发生反应 B、导致产品氢氧化钠中混有杂质,难以分离.
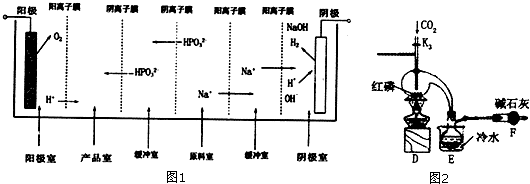
(3)三氯化磷(PC13)是一种重要的有机合成催化剂,实验室常用红磷与干燥的Cl2制取PC13,装置如图2所示.PCl3遇02会生成POCl3 (三氯氧磷),POCl3溶于PC13,PC13遇水会强烈水解生成亚磷酸和HCl,PCl3、POCl3的熔沸点见如表.
请回答:
①E烧杯内冷水的作用是冷凝PCl3蒸汽,便于PCl3收集.
②干燥管F的作用是收尾气中氯气,以免污染空气,防止空气中的水蒸气进入烧瓶使PCl3水解.
③检査装置气密性后,向D装置的曲颈瓶中加人红磷,打开K3通人干燥的CO2,一段时间后关闭K3,加热曲颈瓶至上部有黄色升华物出现时通人氯气,反应立即进行,其中通人干燥CO2的目的是排尽曲颈瓶中的空气,防止PC13与O3等发生副反应.
(4)实验制得的粗产品中常含有POC13、PC15等,加入红磷加热除去PC15后,再通过蒸馏(填实验名称)即可得到较纯净的PC13.
(1)其中次磷酸钠常用来给腈纶织物进行化学镀,某种碱性化学镀铜试剂的配方有次磷酸钠和硫酸铜,产物中有亚磷酸钠的正盐,请写出相关离子方程式:H2PO2-+Cu2++3OH-=Cu↓+HPO32-+2H2O.
(2)亚磷酸可以由三氯化磷水解得到,也可以由电解亚磷酸钠来制备,如图1是用一个六室电渗析槽制备亚磷酸.其中阳极室和产品室之间的阳离子膜主要目的是防止:2H3PO3+O2=2H3PO4(只要求写出化学方程式),这种方法的产品除了有亚磷酸,还有:氧气、氢气、氢氧化钠,如果去掉右边两个阳离子膜(没有了右边的缓冲室),带来的不利后果是(填序号):B.
A、氢氧化钠与原料Na2HP03会发生反应 B、导致产品氢氧化钠中混有杂质,难以分离.

(3)三氯化磷(PC13)是一种重要的有机合成催化剂,实验室常用红磷与干燥的Cl2制取PC13,装置如图2所示.PCl3遇02会生成POCl3 (三氯氧磷),POCl3溶于PC13,PC13遇水会强烈水解生成亚磷酸和HCl,PCl3、POCl3的熔沸点见如表.
| 物质 | 熔点/℃ | 沸点/℃ |
| PC13 | -112 | 75.5 |
| POCI3 | 2 | 105.3 |
①E烧杯内冷水的作用是冷凝PCl3蒸汽,便于PCl3收集.
②干燥管F的作用是收尾气中氯气,以免污染空气,防止空气中的水蒸气进入烧瓶使PCl3水解.
③检査装置气密性后,向D装置的曲颈瓶中加人红磷,打开K3通人干燥的CO2,一段时间后关闭K3,加热曲颈瓶至上部有黄色升华物出现时通人氯气,反应立即进行,其中通人干燥CO2的目的是排尽曲颈瓶中的空气,防止PC13与O3等发生副反应.
(4)实验制得的粗产品中常含有POC13、PC15等,加入红磷加热除去PC15后,再通过蒸馏(填实验名称)即可得到较纯净的PC13.
20.“类推”的思维方式在化学学习与研究中经常采用,但有时会产生错误结论.下列类推结论中,正确的是
( )
( )
| A. | 由氢氟酸刻蚀玻璃可推知盐酸也能用来刻蚀玻璃 | |
| B. | 由钠与冷水剧烈反应,可推知钾也能与冷水剧烈反应 | |
| C. | 由Na2O中阴阳离子个数比为1:2,可推出Na2O2中阴阳离子个数比为 1:1 | |
| D. | 由“2Fe+3Br2=2FeBr3”反应可推出“2Fe+3I2=2FeI3”反应也能发生 |
 硫-碘循环分解水制氢主要涉及下列反应:
硫-碘循环分解水制氢主要涉及下列反应: