题目内容
14.配制250mL 0.0500mol•L-1的Na2CO3溶液,不需要的仪器有( )| A. | 锥形瓶 | B. | 250 mL容量瓶 | C. | 烧杯 | D. | 玻璃棒 |
分析 根据配制一定量物质的量浓度溶液的实验操作步骤选择合适的仪器,据此解答.
解答 解:配制250mL 0.0500mol•L-1的Na2CO3溶液,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到250mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所用仪器有托盘天平、烧杯、玻璃棒、250mL容量瓶、胶头滴管、药匙,不需要锥形瓶;
故选:A.
点评 本题考查了配制一定量物质的量浓度溶液的操作时仪器的选取,明确配制原理及操作步骤是解题关键,题目难度不大.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
5.从下列叙述中,可以肯定金属A比金属B的活动性强的是( )
| A. | A原子的最外层电子数比B原子的最外层电子数少 | |
| B. | B的最高价氧化物水化物的碱性强于A的最高价氧化物水化物的碱性 | |
| C. | 1molA与酸反应生成的H2比1molB与酸反应生成的H2多 | |
| D. | 常温时,A能从水中置换出氢气,而B不能 |
2.下列反应中,化学反应速率最快的是( )
| A. | 硝酸见光分解 | B. | 硝酸银溶液与盐酸反应 | ||
| C. | 钢铁生锈 | D. | 白薯发酵制白酒 |
9.向30mL 1mol•L-1的AlCl3溶液中逐渐加入浓度为4mol•L-1的NaOH溶液,若产生0.78g白色沉淀,则加入的NaOH溶液的体积可能为( )
| A. | 27.5 mL | B. | 17.5 mL | C. | 15 mL | D. | 3 mL |
3.下列各组中的离子,能在溶液中大量共存的是( )
| A. | Cu2+、Ba2+、Cl-、SO42- | B. | Na+、Fe3+、SO42-、OH- | ||
| C. | H+、Na+、CO32-、NO3- | D. | K+、Na+、Cl-、OH- |
4.若NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 16 g CH4与18 g NH4+所含质子数相等 | |
| B. | 常温下,5.6g 铁钉与足量浓硝酸反应,转移的电子数为0.3 NA | |
| C. | 1L 0.5 mol•L-1 Na2CO3溶液中,阴阳离子总数为1.5 NA | |
| D. | 常温常压下,11g CO2气体中所含的分子数为0.25NA |
 已知在酸性条件下有以下反应:①2BrO3-+I2═2IO3-+Br2;②2IO3-+10Br-+12H+═I2+5Br2+6H2O.
已知在酸性条件下有以下反应:①2BrO3-+I2═2IO3-+Br2;②2IO3-+10Br-+12H+═I2+5Br2+6H2O.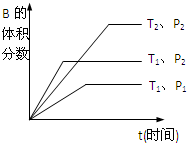 (1)已知某可逆反应mA(g)+nB(g)?qC(g)在密闭容器中进行.如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线.根据图象填空
(1)已知某可逆反应mA(g)+nB(g)?qC(g)在密闭容器中进行.如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线.根据图象填空