题目内容
20.市售的漂粉精的有效成分是Ca(ClO)2,它在潮湿的空气里,发生化学反应的方程式是Ca(ClO)2+2CO2+2H2O=Ca(HCO3)2+2HClO,写出工业上制取漂粉精的化学方程式:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.将氯气制成漂粉精的主要目的是:便于储存和运输.分析 漂粉精的主要成分是次氯酸钙和氯化钙,有效成分是次氯酸钙,利用氯气与石灰乳为原料制备漂粉精,氯气与石灰乳反应生成氯化钙、次氯酸钙与水,漂粉精的主要成分是次氯酸钙和氯化钙.氯化钙没有漂白性,由于次氯酸的酸性比碳酸弱,次氯酸钙能与二氧化碳和水反应生成具有漂白性的次氯酸,漂粉精的有效成分是次氯酸钙,
解答 解:漂粉精的主要成分是次氯酸钙和氯化钙,有效成分是次氯酸钙,由于次氯酸的酸性比碳酸弱,次氯酸钙能与二氧化碳和水反应生成具有漂白性的次氯酸,反应的为:Ca(ClO)2+2CO2+2H2O=Ca(HCO3)2+2HClO,利用氯气与石灰乳为原料制备漂粉精,氯气与石灰乳反应生成氯化钙、次氯酸钙与水,反应的化学方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,将氯气制成漂粉精的主要目的是便于储存和运输,
故答案为:Ca(ClO)2,Ca(ClO)2+2CO2+2H2O=Ca(HCO3)2+2HClO,2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O、便于储存和运;
点评 本题考查物质的组成,物质性质的理解应用和制备方法,题目难度不大,注意相关基础知识的积累.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.下列条件下化学反应速率最大的是( )
| A. | 20℃0.1mol•L-1的盐酸溶液20 mL与0.5g块状碳酸钙反应 | |
| B. | 20℃0.2mol•L-1的盐酸溶液10mL与0.5g粉状碳酸钙反应 | |
| C. | 10℃0.2mol•L-1的盐酸溶液10mL与0.5g粉状碳酸钙反应 | |
| D. | 10℃0.1mol•L-1的盐酸溶液20 mL与1g块状碳酸钙反应 |
11.常用两种方法制备氯化物:①金属与氯气直接化合;②金属与盐酸反应.上述两种方法都可制得的氯化物是( )
| A. | CuCl2 | B. | ZnCl2 | C. | FeCl3 | D. | AlCl3 |
8.在下列各变化过程中,一定要加还原剂才能实现的是( )
| A. | HNO3→NO | B. | H2S→S | C. | FeCl2→FeCl3 | D. | SO32-→SO2 |
15.下列关于摩尔的说法中,正确的是( )
| A. | 是物质的量 | B. | 是一个物理量 | ||
| C. | 是一种物理量的单位 | D. | 是摩尔质量 |
5.下列有关化学实验操作正确的是( )
| A. |  称取NaOH固体 | B. |  稀释浓H2SO4 | ||
| C. |  将乙醇与水分离 | D. | 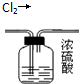 除去氯气中的水蒸气 |
10.下列物质中不能发生银镜反应的是( )
| A. | 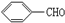 | B. | HCOOH | C. | HCOOC2H5 | D. |  |
