题目内容
(1)已知反应及几种物质中化学键断裂时的能量变化如下所示:
H2(g)+Cl2(g)=2HCl(g) △H=-184kJ/mol
4HCl (g)+O2(g)=2Cl2 (g) +2H2O (g) △H=-115.6kJ/mol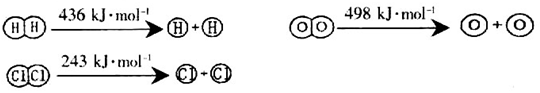
①H2与O2反应生成气态水的热化学方程式为_________________________________;
②断开1mol H—O键所需能量约为_________________________kJ。
(2)已知某反应的平衡常数表达式为:K= ,它所对应的化学方程式为________________。
,它所对应的化学方程式为________________。
(3)已知反应N2(g)+3H2(g) 2NH3(g) △H<0在400℃时K=0.5,此条件下在0.5L的密闭容器中进行该反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应υ(N2)正______υ(N2)逆(填“>”、“<”或“=”)。欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积百分数增加,可采取的措施是_______(填序号)。
2NH3(g) △H<0在400℃时K=0.5,此条件下在0.5L的密闭容器中进行该反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应υ(N2)正______υ(N2)逆(填“>”、“<”或“=”)。欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积百分数增加,可采取的措施是_______(填序号)。
A.缩小体积增大压强 B.升高温度
C.加催化剂 D.使氨气液化移走
(4)在一定体积的密闭容器中进行如下化学反应:A(g)+3B(g) 2C(g)+D(s) △H,其化学平衡常数K与T的关系如下表:
2C(g)+D(s) △H,其化学平衡常数K与T的关系如下表:
| T/K | 300 | 400 | 500 | …… |
| K/(mol·L-1)2 | 4×106 | 8×107 | 1.2×109 | …… |
②在一定条件下,能判断该反应一定达化学平衡状态的是______(填序号)。
A.3 υ(B)正=2υ(C)逆 B.A和B的转化率相等
C.容器内压强保持不变 D.混合气体的密度保持不变
(1)①2H2(g)+O2(g)=2H2O (g) △H=-483.6kJ/mol(2分)②463.4(1分)
(2)C(s)+H2O(g) CO(g)+H2(g)(1分,不标状态不扣分,写成等号不给分)
CO(g)+H2(g)(1分,不标状态不扣分,写成等号不给分)
(3)=(1分);A(1分)(4)①>(1分)②CD(1分)
解析试题分析:(1)①已知热化学方程式a:H2(g)+Cl2(g)=2HCl(g) △H=-184kJ/mol,b:4HCl (g)+O2(g)=2Cl2 (g) +2H2O (g) △H=-115.6kJ/mol,则根据盖斯定律可知,a×2+b即得到反应2H2(g)+O2(g)=2H2O (g) (g),所以该反应的反应热△H=-184kJ/mol×2-115.6kJ/mol=-483.6kJ/mol。
②断裂1molH-H键需要的能量是436kJ,而断裂1molO=O键需要的能量是498kJ。由于反应热还等于断键吸收的能量和形成化学键所放出的能量的差值,所以根据氢气燃烧的热化学方程式可知2×436kJ+498kJ-2×2×x=-483.6kJ,解得x=463.4kJ,因此断开1mol H—O键所需能量约为463.4kJ。
(2)化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以依据平衡常数表达式K= 可知,该反应的方程式为C(s)+H2O(g)
可知,该反应的方程式为C(s)+H2O(g) CO(g)+H2(g)。
CO(g)+H2(g)。
(3)一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,其浓度分别是(mol/L)4、2、4。则此时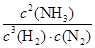 =
=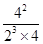 =0.5,这说明反应达到平衡状态,所以此时反应υ(N2)正=υ(N2)逆;A、正方应是体积减小的,则缩小体积增大压强,反应速率加快,平衡向正反应方向移动,氨气的含量增大,A正确;B、正方应是放热反应,升高温度反应速率加快,平衡向逆反应方向移动,氨气含量降低,B不正确;C、加催化剂加快反应速率,但平衡状态不变,氨气含量不变,C不正确;D、使氨气液化移走,平衡向正反应方向移动,但则反应速率降低,D不正确,答案选A。
=0.5,这说明反应达到平衡状态,所以此时反应υ(N2)正=υ(N2)逆;A、正方应是体积减小的,则缩小体积增大压强,反应速率加快,平衡向正反应方向移动,氨气的含量增大,A正确;B、正方应是放热反应,升高温度反应速率加快,平衡向逆反应方向移动,氨气含量降低,B不正确;C、加催化剂加快反应速率,但平衡状态不变,氨气含量不变,C不正确;D、使氨气液化移走,平衡向正反应方向移动,但则反应速率降低,D不正确,答案选A。
(4)①根据表中数据可知,随着温度的升高,平衡常数逐渐增大。这说明升高温度平衡向正反应方向进行,所以正方应是吸热反应,即△H>0。
②在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,据此可以判断。A、由于反应速率之比是相应的化学计量数之比,则3 υ(B)正=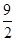 υ(C)正=2υ(C)逆,因此正逆反应速率不等,没有达到平衡状态,A不正确;B、A和B的转化率相等不能说明正逆反应速率相等,即反应不一定达到平衡状态,所以B不正确;C、正方应是体积减小的可逆反应,因此压强始终是减小,所以当容器内压强保持不变时可以说明反应达到平衡状态,C正确;D、密度是混合气的质量和容器容积的比值,在反应过程中容积始终是不变的,但气体的质量是减小的,所以当混合气体的密度保持不变时,可以说明反应达到平衡状态,D正确,答案选CD。
υ(C)正=2υ(C)逆,因此正逆反应速率不等,没有达到平衡状态,A不正确;B、A和B的转化率相等不能说明正逆反应速率相等,即反应不一定达到平衡状态,所以B不正确;C、正方应是体积减小的可逆反应,因此压强始终是减小,所以当容器内压强保持不变时可以说明反应达到平衡状态,C正确;D、密度是混合气的质量和容器容积的比值,在反应过程中容积始终是不变的,但气体的质量是减小的,所以当混合气体的密度保持不变时,可以说明反应达到平衡状态,D正确,答案选CD。
考点:考查反应热的计算、平衡常数的应用、外界条件对反应速率和平衡状态的影响以及平衡状态的判断

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案我国工业上主要采用以下四种方法降低尾气中的含硫量:
| 方法1 | 燃煤中加入石灰石,将SO2转化为CaSO3,再氧化为CaSO4 |
| 方法2 | 用氨水将SO2转化为NH4HSO3,再氧化为(NH4)2SO4 |
| 方法3 | 高温下用水煤气将SO2还原为S |
| 方法4 | 用Na2SO3溶液吸收SO2,再电解转化为H2SO4 |
(1)方法1中已知:① CaO(s)+CO2(g)=CaCO3(s) ΔH=-178.3 kJ/mol
②CaO(s)+SO2(g)=CaSO3(s) ΔH=-402.0 kJ/mol
③2CaSO3(s)+O2(g)=2CaSO4(s) ΔH=-2314.8 kJ/mol
写出CaCO3与SO2反应生成CaSO4的热化学方程式:____;此反应的平衡常数表达式为:_____。
(2)方法2中最后产品中含有少量(NH4)2SO3,为测定(NH4)2SO4的含量,分析员设计以下步骤:
①准确称取13.9 g 样品,溶解;
②向溶液中加入植物油形成油膜,用滴管插入液面下加入过量盐酸,充分反应,再加热煮沸;
③加入足量的氯化钡溶液,过滤;
④进行两步实验操作;
⑤称量,得到固体23.3 g,计算。
步骤②的目的是:_____。步骤④两步实验操作的名称分别为: _____、_____。样品中(NH4)2SO4的质量分数:____(保留两位有效数字)。
(3)据研究表明方法3的气配比最适宜为0.75[即煤气(CO、H2的体积分数之和为90%)∶SO2烟气(SO2体积分数不超过15%)流量=30∶40]。用平衡原理解释保持气配比为0.75的目的是:_____。
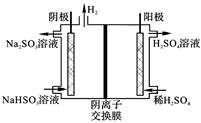
(4)方法4中用惰性电极电解溶液的装置如图所示。阳极电极反应方程式为_____。
废旧印刷电路板的回收利用可实现资源再生,并减少污染。废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末。
(1)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是 (填字母)。
| A.热裂解形成燃油 | B.露天焚烧 | C.作为有机复合建筑材料的原料 | D.直接填埋 |
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H=64.39kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) △H=-196.46kJ·mol-1
H2(g)+1/2O2(g)=H2O(l) △H=-285.84kJ·mol-1

在 H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为 。
(3)控制其他条件相同,印刷电路板的金属粉末用10℅H2O2和3.0mol·L-1H2SO4的混合溶液处理,测得不同温度下铜的平均溶解速率(见下表)。
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜平均溶解速率(×10-3 mol·L-1·min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是 。
(4)在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀。制备CuCl的离子方程式是 。
(5) 已知相同条件下:
4Ca5(PO4)3F(s)+3SiO2(s)=6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g) ;△H1
2Ca3(PO4)2(s)+10C(s)=P4(g)+6CaO(s)+10CO(g);△H2
SiO2(s)+CaO(s)=CaSiO3(s) ;△H3
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)=3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g) ;
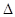 H
H
用△H1、△H2和△H3表示
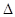 H,
H,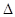 H= 。
H= 。(6)已知1 g FeS2(s)完全燃烧生成放出7.1 kJ热量,FeS2燃烧反应的热化学方程式为 。
 CH3OH(g) ΔH
CH3OH(g) ΔH
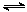 CH3OH(g) △H 1=-90.7 kJ·mol-1
CH3OH(g) △H 1=-90.7 kJ·mol-1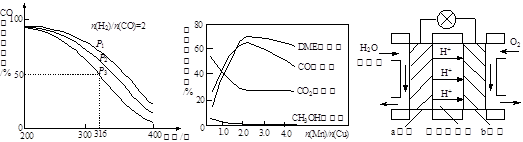
 CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。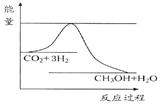
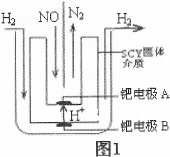
 4N2(g)+6H2O(g) (△H <0)
4N2(g)+6H2O(g) (△H <0)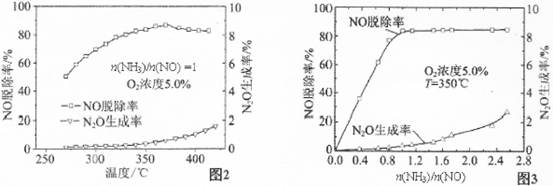
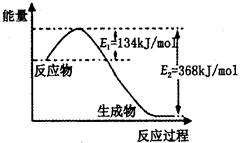
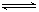 2NH3(g)△H<0,其平衡常数K与温度T的关系如下表:
2NH3(g)△H<0,其平衡常数K与温度T的关系如下表: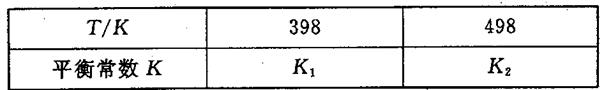
 2H2O(l) △H=-483.6 kJ/mol
2H2O(l) △H=-483.6 kJ/mol CH3OH(g)。工业上依此用CO生产燃料甲醇。
CH3OH(g)。工业上依此用CO生产燃料甲醇。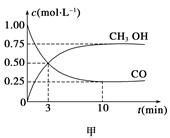
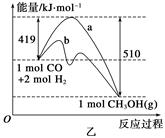
 增大的有____________。
增大的有____________。