题目内容
7.三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物.探究过程如下:查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,Cu2O在空气中加热生成CuO
提出假设
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂.
(1)若假设1成立,则实验现象是固体完全溶解,溶液呈血红色.
(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?不合理;当原固体粉末为Fe2O3和Cu2O的混合物时,加入稀H2SO4后产生的Fe3+与Cu反应生成Fe2+,滴加KSCN溶液后也可能不变红色.
(3)若固体粉末完全溶解无固体存在,滴加 KSCN 试剂时溶液不变红色,则证明原固体粉末是Fe2O3和Cu2O,写出发生反应的离子方程式Fe2O3+6H+=2Fe3++3H2O、Cu2O+2H+═Cu+Cu2++H2O、2Fe3++Cu═2Fe2++Cu2+.
探究延伸
经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物.
(4)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为$\frac{9(b-a)}{a}$×100%.
(5)欲利用红色粉末Fe2O3和Cu2O的混合物制取较纯净的胆矾 (CuSO4.5H2O)经查阅资料得知,在溶液中调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
A.氯水 B.H2O2 C.硝酸 D.NaOH E.氨水 F.Cu2(OH)2CO3
实验小组设计如下实验方案:

试回答:①试剂I为B,试剂II为F(填字母).
②固体X的化学式为Fe(OH)3.
分析 (1)依据假设1为氧化铁,和实验工厂分析,固体溶解后生成硫酸铁,遇到硫氰酸钾会发生反应生成血红色溶液;
(2)滴加KSCN试剂后液不变红色,说明溶液中无铁离子,可能是氧化亚铜在酸中发生氧化还原反应生成氧化铜和铜,生成的铜能把铁离子还原为亚铁离子,使溶液遇到硫氰酸钾不变红色;
(3)固体完全溶解,无固体存在,说明固体含有氧化铁和氧化亚铜;反应生成的铜会和铁离子全部反应;
(4)依据题意,能发生反应的物质为Cu2O,最后变成CuO,增加的质量就是反应的氧气的质量,根据质量差计算可以得出Cu2O的质量分数;
(5)①红色粉末为Fe2O3和Cu2O的混合物溶于硫酸后氧化亚铜反应生成的铜会还原铁离子为亚铁离子,加入氧化剂过氧化氢氧化亚铁离子为铁离子,调节溶液PH使铁离子全部沉淀;
②X推断为氢氧化铁沉淀;
③操作1是溶液中得到溶质结晶水合物;是通过蒸发浓缩冷却结晶,过滤洗涤干燥得到晶体;
解答 解:(1)取少量粉末放入足量稀硫酸中.在所得溶液中再滴加KSCN试剂,若假设1成立,红色粉末是Fe2O3,则实验现象是固体完全溶解,溶液呈血红色;
故答案为:固体完全溶解,溶液呈血红色;
(2)滴加KSCN试剂后溶液不变红色,说明溶液中无铁离子,可能是氧化亚铜在酸中发生氧化还原反应生成氧化铜和铜,生成的铜能把铁离子还原为亚铁离子,使溶液遇到硫氰酸钾不变红色,所以滴加KSCN试剂后溶液不变红色,不能说明原混合物不含氧化铁;
故答案为:不合理;当原固体粉末为Fe2O3和Cu2O的混合物时,加入稀H2SO4后产生的Fe3+与Cu反应生成Fe2+,滴加KSCN溶液后也可能不变红色;
(3)固体完全溶解,无固体存在,说明固体含有氧化铁和氧化亚铜;反应生成的铜会和铁离子全部反应,反应的离子方程式为:Cu2O+2H+═Cu+Cu2++H2O、2Fe3++Cu═2Fe2++Cu2+;
故答案为:Fe2O3和Cu2O;Cu2O+2H+═Cu+Cu2++H2O、2Fe3++Cu═2Fe2++Cu2+;
(4)依据题意,能发生反应的物质为Cu2O,最后变成CuO,增加的质量就是反应的氧气的质量,根据质量差计算可以得出Cu2O的质量分数.
设样品中氧化亚铜的质量为m,
2Cu2O+O2═4CuO△m
288g 32g
m (b-a)g
m=$\frac{288×(\\;b-a)g}{32g}$=9(b-a)g,
混合物中Cu2O的质量分数为$\frac{9(b-a)}{a}$×100%,
故答案为:$\frac{9(b-a)}{a}$×100%.
(5)①红色粉末为Fe2O3和Cu2O的混合物溶于硫酸后氧化亚铜反应生成的铜会还原铁离子为亚铁离子,加入氧化剂过氧化氢氧化亚铁离子为铁离子,调节溶液PH使铁离子全部沉淀,为不引入杂质需要加入氧化铜或碱式碳酸铜调节溶液PH,ACDE会引入新的杂质;
故答案为:B;F;
②流程分析判断固体X为氢氧化铁沉淀;
故答案为:Fe(OH)3;
点评 本题考查了实验探究物质组成和性质的实验分析,物质的性质和转化关系,掌握基础,细心审题是解题关键,题目难度中等.

| A. | 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 | |
| B. | 配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌条件下慢慢加入浓硫酸 | |
| C. | 酒精灯着火时可用沙子扑灭 | |
| D. | 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸 |
| A. | SO2+2NaOH═Na2SO3+H2O | |
| B. | 2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ | |
| C. | 2FeCl3+Fe═3FeCl2 | |
| D. | MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑ |
| A. | 化学反应均伴随着能量的变化 | |
| B. | 需要加热才能发生的反应不一定是吸热反应 | |
| C. | 物质的化学能可以在一定条件下转化为热能、电能为人类利用 | |
| D. | 吸热反应中由于反应物总能量小于生成物总能量,因而没有利用价值 |
| A. | SiO2→H2SiO3、CuO→Cu(OH)2、CuSO4→CuCl2均不能通过一步反应实现 | |
| B. | FeS、FeCl2、Fe(OH)3均可以通过化合反应制得 | |
| C. | 水在化学反应中可能只做氧化剂、或只做还原剂、或既不做氧化剂也不做还原剂、或既做氧化剂又做还原剂 | |
| D. | 在某一复分解反应中,也有可能弱酸是反应物,而强酸是生成物 |
| A. | 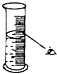 读数 | B. |  稀释 | C. | 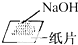 称量 | D. | 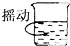 溶解 |