题目内容
【题目】某同学用KSCN溶液和![]() 溶液探究
溶液探究![]() 的还原性时出现异常现象,实验如下:
的还原性时出现异常现象,实验如下:
|
|
|
|
|
|
溶液变红,大约10秒左右红色褪去,有气体生成 | 溶液变红且不褪色,有气体生成 | 溶液变红且不褪色,滴加盐酸和 |
下列说法不正确的是
A.对比![]() ,可以判定酸性条件下
,可以判定酸性条件下![]() 可以氧化
可以氧化![]()
B.实验![]() 中发生的氧化还原反应有两种
中发生的氧化还原反应有两种
C.![]() 中红色溶液中含有
中红色溶液中含有![]() 胶体
胶体
D.![]() 中发生的氧化还原反应为:
中发生的氧化还原反应为:![]()
【答案】B
【解析】
![]() 盐酸酸化的氯化亚铁溶液中滴入KSCN溶液,
盐酸酸化的氯化亚铁溶液中滴入KSCN溶液,![]() ,滴入过氧化氢发生氧化还原反应,生成铁离子,形成血红色溶液,大约10秒左右红色褪去,铁离子做催化剂过氧化氢分解有气体生成
,滴入过氧化氢发生氧化还原反应,生成铁离子,形成血红色溶液,大约10秒左右红色褪去,铁离子做催化剂过氧化氢分解有气体生成![]() 经检验为
经检验为![]() ,取褪色后溶液,滴加盐酸和
,取褪色后溶液,滴加盐酸和![]() 溶液,产生白色沉淀为硫酸钡沉淀,证明
溶液,产生白色沉淀为硫酸钡沉淀,证明![]() 离子被氧化为硫酸根离子,
离子被氧化为硫酸根离子,
![]() 盐酸酸化的氯化亚铁溶液中滴入KSCN溶液,
盐酸酸化的氯化亚铁溶液中滴入KSCN溶液,![]() ,滴入过氧化氢溶液,溶液变红且不褪色,说明亚铁离子被氧化为铁离子,铁离子对过氧化氢起到催化剂作用,有气体生成
,滴入过氧化氢溶液,溶液变红且不褪色,说明亚铁离子被氧化为铁离子,铁离子对过氧化氢起到催化剂作用,有气体生成![]() 经检验为
经检验为![]() ,经检验有丁达尔效应,说明生成了氢氧化铁胶体,
,经检验有丁达尔效应,说明生成了氢氧化铁胶体,
![]() 盐酸酸化的氯化亚铁溶液中滴入KSCN溶液,
盐酸酸化的氯化亚铁溶液中滴入KSCN溶液,![]() ,通入足量氧气,溶液变红且不褪色,说明氧气氧化亚铁离子生成铁离子,滴加盐酸和
,通入足量氧气,溶液变红且不褪色,说明氧气氧化亚铁离子生成铁离子,滴加盐酸和![]() 溶液,无白色沉淀,经检验无丁达尔效应,无硫酸钡沉淀生成和氢氧化铁胶体形成,排除了氧气氧化
溶液,无白色沉淀,经检验无丁达尔效应,无硫酸钡沉淀生成和氢氧化铁胶体形成,排除了氧气氧化![]() 的可能。
的可能。
A.对比![]() ,实验
,实验![]() 确定了
确定了![]() 离子被氧化为硫酸根离子,实验
离子被氧化为硫酸根离子,实验![]() 排除了氧气氧化
排除了氧气氧化![]() 的可能,可以判定酸性条件下
的可能,可以判定酸性条件下![]() 可以氧化
可以氧化![]() ,故A正确;
,故A正确;
B.实验![]() 中发生的氧化还原反应有亚铁离子被过氧化氢氧化为铁离子,过氧化氢分解生成氧气,氧气氧化亚铁离子,不止两种,故B错误;
中发生的氧化还原反应有亚铁离子被过氧化氢氧化为铁离子,过氧化氢分解生成氧气,氧气氧化亚铁离子,不止两种,故B错误;
C.![]() 中检验有丁达尔效应,说明红色溶液中含有
中检验有丁达尔效应,说明红色溶液中含有![]() 胶体,故C正确;
胶体,故C正确;
D.![]() 中通入足量氧气溶液变红色说明生成了铁离子,发生的氧化还原反应为:
中通入足量氧气溶液变红色说明生成了铁离子,发生的氧化还原反应为:![]() ,故D正确;
,故D正确;
故选:B。

【题目】某同学进行下列实验:
装置 | 操作 | 现象 |
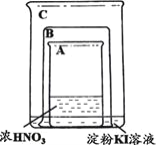
| 将盛有浓硝酸的烧杯A放入盛有淀粉KI溶液的烧杯C中,然后将铜片放入烧杯A后,立即用烧杯B罩住。 | 烧杯A液体上方立即出现大量红棕色气体;一段时间后,红棕色气体消失,烧杯A和C中的液体都变成蓝色。 |
下列说法不合理的是
A.烧杯A中发生反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
B.红棕色气体消失可能与NO2和烧杯C中的KI发生反应有关
C.烧杯A中溶液变蓝是因为产生了Cu(NO3)2
D.若将铜片换成铁片,则C中的液体不会变蓝
【题目】下列实验中的操作,对应的现象以及结论都正确的是![]()
![]()
选项 | 操作 | 现象 | 结论 |
A | 向 | 产生白色沉淀 |
|
B | 蘸有浓氨水的玻璃捧靠近X | 有白烟产生 | X一定是浓盐酸 |
C | 向澄清石灰水加入某试剂的溶液少许 | 产生白色沉淀 | 该试剂中一定含有 |
D | 炭粉中加入浓硫酸并加热,导出的气体通入 | 有白色沉淀产生 | 有 |
A.AB.BC.CD.D