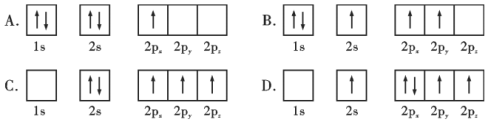
题目内容
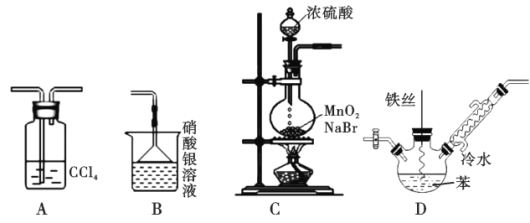
【题目】某化学小组欲利用如图所示的实验装置探究苯与液溴的反应(装置连接顺序为CDAB)
已知:MnO2+2NaBr+2H2SO4![]() Br2↑+MnSO4+Na2SO4+2H2O,下列说法不正确的是
Br2↑+MnSO4+Na2SO4+2H2O,下列说法不正确的是
A. 装置A的作用是除去HBr中的溴蒸气
B. 装置B的作用是检验HBr
C. 可以用装置C制取溴蒸气
D. 装置D反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
【答案】D
【解析】
装置C中二氧化锰、溴化钠和硫酸反应制得溴蒸气,溴蒸气通入装置D中与苯发生取代反应生成溴苯和溴化氢,溴化氢气体中混有溴蒸气和挥发出的苯,溴蒸气会干扰溴化氢的检验,装置A中四氯化碳吸收溴蒸气和挥发出的苯,防止溴蒸气会干扰溴化氢的检验,装置B中溴化氢与硝酸银溶液反应生成淡黄色溴化银沉淀,检验反应有溴化氢生成。
A项、装置A的作用是除去HBr中的溴蒸气,防止溴蒸气会干扰溴化氢的检验,故A正确;
B项、装置B中溴化氢与硝酸银溶液反应生成淡黄色溴化银沉淀,检验反应有溴化氢生成,故B正确;
C项、装置C中二氧化锰、溴化钠和硫酸反应制得溴蒸气,故C正确;
D项、装置D中制得的不溶于水的溴苯中混有溴和苯,经水洗、稀碱溶液洗涤、水洗、分液、干燥、分馏得到溴苯,故D错误;
故选D。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案【题目】下表为元素周期表的一部分,请参照元素①—⑩在表中的位置,用相应的化学用语回答下列问题;
① | |||||||
② | ③ | ④ | ⑤ | ||||
⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中用序号标出的10种元素中,非金属性最强元素的离子结构示意图是____________。
(2)④、⑦、⑩的离子半径由大到小的顺序为____________(用元素符号作答)。
(3)由表中④、⑥元素可以组成一种淡黄色的物质,画出该物质的电子式____________,该物质含有的化学键类型有____________。
(4)元素②的简单气态氢化物为X,0.1molX完成燃烧生成稳定氧化物时放出akJ的能量,写出X燃烧热的热化学方程式:____________。
(5)写出实验室制备氨气的反应方程式____________。
(6)一种氢气燃料电池的原理如图:
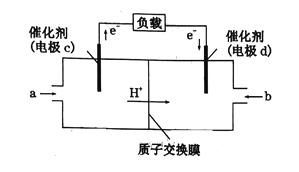
a极通入的气体是____________,正极的电极反应式为____________。
【题目】下表列出了5种元素在周期表中的位置。
族 周期 | ⅠA | 0 | ||||||
1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ |
(1)①的元素符号是_______,⑤的原子结构示意图是__________;
(2)以上元素中,非金属性最强的是___________(填元素符号);
(3)④元素的最高价氧化物对应的水化物呈______性(填“酸”或“碱”或“两”);
(4)③④⑤三种元素按原子半径由大到小的顺序是______(填元素符号);
(5)元素①与元素②的单质氧化性较强的是________(填化学式)。;
(6)元素④的最高价氧化物与元素③的最高价氧化物对应的水化物相互反应的化学方程式__。