题目内容
【题目】
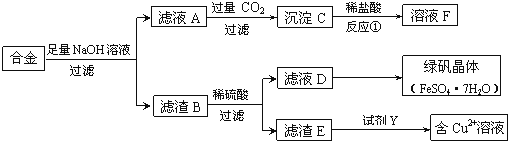
(1)合金与足量氢氧化钠溶液反应的离子方程式是 。
(2)若D中含有Fe3+,除去Fe3+的常用试剂是 。
(3)若要从滤液D中得到绿矾晶体,必须进行的实验操作步骤: 、冷却结晶、过滤、自然干燥。
(4)若由滤渣E得到含Cu2+的溶液,试剂Y可能是 (填选项字母)。
A.稀硝酸 | B.浓硫酸 | C.浓盐酸 | D.稀硫酸 |
根据所选试剂写出一个由滤渣E得到含Cu2+溶液的化学方程式: 。
【答案】(1)2Al+2OH-+2H2O=2AlO2-+3H2↑;(2)铁粉; (3)蒸发浓缩;(4)AB;Cu+2H2SO4![]() CuSO4+SO2↑+2H2O(或3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O)。
CuSO4+SO2↑+2H2O(或3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O)。
【解析】试题分析:(1)合金中只有铝和氢氧化钠发生反应,其离子反应方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑;(2)根据目标产物以及Fe及其化合物的性质,Fe+2Fe2+=3Fe3+,因此加入铁粉;(3)应是蒸发浓缩,减少FeSO4·7H2O的损耗;(4)Cu能和硝酸和浓硫酸反应,因此选AB;Cu+2H2SO4![]() CuSO4+SO2↑+2H2O(或3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O)。
CuSO4+SO2↑+2H2O(或3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O)。

练习册系列答案
相关题目
【题目】常温下,下列各组物质中,Y既能与X反应又能与Z反应的是( )
X | Y | Z | |
① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
② | KOH溶液 | SiO2 | 浓盐酸 |
③ | O2 | N2 | H2 |
④ | FeCl3溶液 | Cu | 浓硝酸 |
A. ①③ B. ①④ C. ②④ D. ②③



