题目内容
【题目】下列关于电化学的实验事实正确的是( )
出现环境 | 实验事实 | |
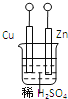
A | 以稀H2SO4为电解质的Cu-Zn原电池 | Cu为正极,正极上发生还原反应 |
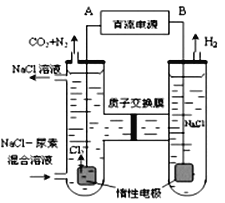
B | 电解CuCl2溶液 | 电子经过负极→阴极 |
C | 弱酸性环境下钢铁腐蚀 | 负极处产生H2,正极处吸收O2 |
D | 将钢闸门与外加电源负极相连 | 牺牲阳极阴极保护法,可防止钢闸门腐蚀 |
【答案】A
【解析】
试题分析:A、锌比铜活泼,锌作负极,反应式为:Zn-2e-=Zn2+,铜作正极,反应式2H++2e-=H2↑,正极上得到电子,化合价降低,发生还原反应,故正确;B、电解过程中,电子从负极流向阴极,从阳极流向正极,电解池内部没有电子通过,只有阴阳离子的定向移动,故错误;C、在弱酸性环境下,发生钢铁析氢腐蚀,铁作负极,反应式Fe-2e-=Fe2+,正极反应式为:2H++2e-=H2↑,故错误;D、牺牲阳极的阴极保护法是在钢闸门上连接一个比铁活泼的金属作负极,钢闸门作正极,故错误。

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
【题目】某同学用NaHCO3和KHCO3组成的混合物进实验,测得的实验数据如下表所示(盐酸的物质的量浓度相同):(计算结果保留3位有效数字)
实验编号 | ① | ② | ③ |
盐酸体积(mL) | 50 | 50 | 50 |
混合物的质量(g) | 9.2 | 15.7 | 27.6 |
标准状况下CO2的体积(L) | 2.24 | 3.36 | 3.36 |
回答下列问题:
(1)由实验______________(填实验编号)可判断盐酸完全反应,理由是_____________。
(2)盐酸的物质的量浓度为__________________。
(3)产生标准状况下3.36LCO2所需固体的质量为______________________。