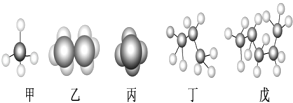
��Ŀ����
����Ŀ�����ڻ�ѧ��Ӧ���ʺ��ȣ�����˵����ȷ���ǣ�
A. �ܱ������н��е����·�Ӧ��2X(g)+Y(g)![]() Z(g)+W(s) ��H��0�������¶ȣ�����Ӧ���������淴Ӧ���ʼ�С
Z(g)+W(s) ��H��0�������¶ȣ�����Ӧ���������淴Ӧ���ʼ�С
B. ���ڷ�Ӧ��H2S(g) ![]() H2(g)��S(s)����H��0 ����ѹ���¶���ʹ��ѧƽ�����淴Ӧ�����ƶ�
H2(g)��S(s)����H��0 ����ѹ���¶���ʹ��ѧƽ�����淴Ӧ�����ƶ�
C. һ�������£�2L �ܱ������д��ڷ�Ӧ��CO(g)+H2O(g)![]() CO2(g)+H2(g) ��H��0����ƽ����ٳ���һ������CO(g)��ƽ�������ƶ���ƽ�ⳣ��K���
CO2(g)+H2(g) ��H��0����ƽ����ٳ���һ������CO(g)��ƽ�������ƶ���ƽ�ⳣ��K���
D. ����Ӧ���Ũ�ȣ�ƽ�������ƶ���������İٷֺ�����һ������
���𰸡�D
��������
A. 2X(g)+Y(g)![]() Z(g)+W(s) ��H��0�������¶ȣ�����Ӱٷ������ӡ����淴Ӧ���ʾ�����A����
Z(g)+W(s) ��H��0�������¶ȣ�����Ӱٷ������ӡ����淴Ӧ���ʾ�����A����
B. ���ڷ�Ӧ��H2S(g) ![]() H2(g)��S(s)����H��0 ����ѹƽ�������ƶ������»�ѧƽ�����淴Ӧ�����ƶ�����B����
H2(g)��S(s)����H��0 ����ѹƽ�������ƶ������»�ѧƽ�����淴Ӧ�����ƶ�����B����
C.ƽ�ⳣ��K�������ֻ���¶�Ӱ�죬�¶Ȳ��䣬ʼ���Ƕ�ֵ����C����
D.����Ӧ���Ũ�ȣ�ƽ�������ƶ���������İٷֺ���=![]() ����Ϊ���ӣ���ĸ����������������İٷֺ�����һ������D��ȷ��
����Ϊ���ӣ���ĸ����������������İٷֺ�����һ������D��ȷ��
��ȷ�𰸣�D��

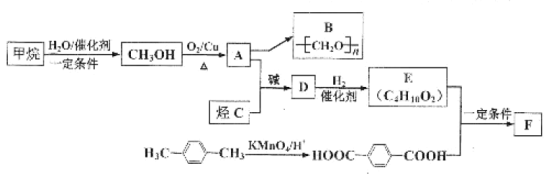
����Ŀ��������(CH3OCH3)��һ��������Դ��
��֪����CO(g)��2H2(g)![]() CH3OH(g) ��H1����99kJ��mol-1
CH3OH(g) ��H1����99kJ��mol-1
��2CH3OH(g)![]() CH3OCH3(g)��H2O(g) ��H2����24kJ��mol-1
CH3OCH3(g)��H2O(g) ��H2����24kJ��mol-1
��CO(g)��H2O(g)![]() CO2(g)��H2(g) ��H3����41kJ��mol-1
CO2(g)��H2(g) ��H3����41kJ��mol-1
�ش��������⣺
��1��д��CO��H2��Ӧ����CO2��CH3OCH3(g)���Ȼ�ѧ����ʽ_____��
��2�����м�����߷�Ӧ���� CO ��ƽ��ת���ʣ���������Ӧ���ʵ���____�����ţ���
a������ѹǿ b�������¶� c������H2Ũ�� d���Ӹ�Ч����
��3����ij���º��������з�����Ӧ�ۣ���˵���÷�Ӧ�ﵽƽ�����___�����ţ���
a������ƽ����Է����������ֲ���
b����H3���ֲ���
c��![]() ���ֲ���
���ֲ���
d�������ܶȱ��ֲ���
��4����һ���¶ȣ�T�棩�£�������ܱ�������ͨ��һ����CH3OH���壬ֻ������Ӧ�ڡ�����������CH3OCH3 �����ʵ�������[��(CH3OCH3)]�뷴Ӧʱ��(t)�й����������ʾ��
t/min | 0 | 15 | 30 | 45 | 80 | 100 |
��(CH3OCH3) | 0 | 0.05 | 0.08 | 0.09 | 0.10 | 0.10 |
�ٸ��¶��£�������Ӧ��ƽ�ⳣ��KΪ___���÷�����ʾ����
�ڷ�Ӧ����v��v����v��������v����k������2(CH3OH)��v����k������(CH3OCH3)����(H2O)��k����k ���ֱ�Ϊ�����淴Ӧ���ʳ�����![]() ֻ���¶��йء�15minʱ����___���������2λС������
ֻ���¶��йء�15minʱ����___���������2λС������
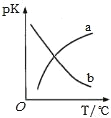
��5�����ܱ������з�����Ӧ�ۣ�ƽ�ⳣ��ΪK��pK��pK����lgK�����¶ȵĹ�ϵ��ͼ��ʾ��ͼ������___���a����b�����ܷ�ӳƽ�ⳣ���仯���ơ�