��Ŀ����
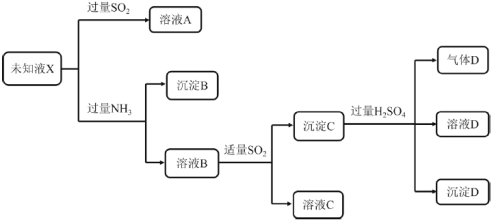
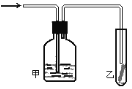
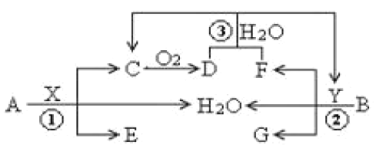
����Ŀ����֪���ֳ�������A(�ؿ��к����ڶ��Ľ���)��B(��ɫ����)�ֱ���������X��Y������Ӧ����ת����ϵ��ͼ��ʾ������DΪ����ɫ���塣
�ش��������⣺
��1����Ӧ�۵����ӷ�Ӧ����ʽΪ___��
��2��6.4gB�����X��Һ(8mol /L��60mL)��ַ�Ӧ�����ɵĻ�ԭ������C��D����Ӧ����Һ������XΪn mol ����ʱ��Һ������X�������ӵ����ʵ���Ϊ___mol��
��3��������A��Y��ϡ��Һ�ܷ�����Ӧ������W�����ڹ���W��ת����ϵ��ͼ��ʾ(����������ȥ)������N�Ǻ���ɫ�Ļ����

��M�����ֻ�������ɣ����к��Уƣ�����ͨ��BaCl2��Һ��ʵ��������___��
��������ӦI�õ�16 g����Σ�����������Mǡ�ñ�0.3L1mol��L��1 NaOH��Һ��ȫ���յ���Һ1����Ӧ���з�����Ӧ�����ӷ���ʽ��____��
���𰸡�SO2+NO2 +H2O=2H++SO42-+NO n+0.2 ������ɫ���� 2Fe3++HSO3-+H2O=2Fe2++SO42-+3H+
��������
��������AΪ�ؿ��к����ڶ��Ľ�����ȷ��ΪFe��BΪ��ɫ����ȷ��ΪCu������ DΪ����ɫ���壬ȷ��DΪNO2��CΪNO��XΪHNO3��BΪCu��ͭ������Ũ���ᷴӦ��������ͭ�����������ˮ�����ɵĶ��������л�ԭ�ԣ�������NO2��Ӧ������������ᣬȷ��BΪCu��YΪ���ᣬFΪSO2��GΪCuSO4����3��A��Fe����Y�����ᣩ��ϡ��Һ��Ӧ��������������������ȷ��WΪFeSO4��2FeSO4![]() Fe2O3+SO2��+SO3��������MΪSO2��SO3�Ļ���M��NaOH��Ӧ�����κ�ˮ��NΪFe2O3����ϡ���ᷴӦ������������ˮ��Fe3+���������Ժ�+4����Ԫ�ؾ��л�ԭ�ԣ����Է���������ԭ��Ӧ���������������ݴ˷�����
Fe2O3+SO2��+SO3��������MΪSO2��SO3�Ļ���M��NaOH��Ӧ�����κ�ˮ��NΪFe2O3����ϡ���ᷴӦ������������ˮ��Fe3+���������Ժ�+4����Ԫ�ؾ��л�ԭ�ԣ����Է���������ԭ��Ӧ���������������ݴ˷�����
��1���������Ϸ�����֪����Ӧ��ΪSO2��NO2��ˮ�ķ�Ӧ�����ݵ�ʧ��������Ⱥ�ԭ���غ���ƽ�������ӷ�Ӧ����ʽΪSO2+NO2 +H2O=2H++SO42-+NO��
�𰸣�SO2+NO2 +H2O=2H++SO42-+NO
��2��6.4gB�����X��Һ(HNO3)��ַ�Ӧ�����ɵĻ�ԭ������NO2��NO����Ӧ����Һ������HNO3Ϊn mol ����Һ������N![]() �����ʵ���Ϊ��n��N
�����ʵ���Ϊ��n��N![]() ��=n��Cu2+����2+n=
��=n��Cu2+����2+n=![]() +n= n+0.2mol��
+n= n+0.2mol��
�𰸣�n+0.2
��3���ٽ��ͣ�SO2��SO3��ͨ��BaCl2��Һ��������ӦSO3+H2O+BaCl2=BaSO4��+2HCl���а�ɫ�������ɣ�
�𰸣�������ɫ����
�ڷ�Ӧ��2FeSO4![]() Fe2O3+ SO2��+ SO3������Ӧ��Fe2O3+3H2SO4=Fe2(SO4)3+3H2O��
Fe2O3+ SO2��+ SO3������Ӧ��Fe2O3+3H2SO4=Fe2(SO4)3+3H2O��
���ݹ���M��Fe2O3�����������SO2��SO3�����ʵ�����
2FeSO4![]() Fe2O3+ SO2��+ SO3��
Fe2O3+ SO2��+ SO3��
160g 1mol 1mol
1.6g 0.01mol 0.01mol
��Ӧ�� SO3 + 2NaOH=Na2SO4+H2O
1mol 2mol 1mol
0.01mol 0.02mol 0.01mol
SO2+ NaOH = NaHSO3
1mol 1mol 1mol
0.01mol 0.01mol 0.01mol
��Һ1ΪNa2SO4��NaHSO3�Ļ���
��Ӧ�������������������ԣ����������ƾ��л�ԭ�ԣ����ݵ�ʧ��������Ⱥ�ԭ���غ�ó����ӷ���ʽ2Fe3++HSO3-+H2O=2Fe2++SO42-+3H+��
�𰸣�2Fe3++HSO3-+H2O=2Fe2++SO42-+3H+

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ����һ��������ܱ������У��������»�ѧ��Ӧ��CO2(g)��H2(g)![]() CO(g)��H2O(g)����H=a kJ��mol��1�仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
CO(g)��H2O(g)����H=a kJ��mol��1�仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t/�� | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
����˵������ȷ����(����)
A.�÷�Ӧ������ӦΪ���ȷ�Ӧ����a<0
B.��ƽ��Ũ�ȷ���c(CO2)��c(H2)=c(CO)��c(H2O)ʱ���¶�Ϊ830 ��
C.��������������ʱ������С������������������ڸ÷�Ӧƽ�������ƶ�
D.��v��(H2)=v��(H2O)ʱ�÷�Ӧ�ﵽ��ѧƽ��״̬