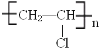题目内容
【题目】有A、B两种烃,它们的组成相同,都约含85.7%的碳,烃A对氢气的相对密度是28;烃B式量比空气的平均式量稍小,且实验式与A相同,烃A、B都能使溴的四氯化碳溶液褪色,根据以上实验事实回答问题。
(1)推断A、B两烃的化学式。
A_____________________________;B_________________________。
(2)A、B中_________(填A、B的结构简式)存在同分异构体,同分异构体的名称是_______________________。(有多少写多少)
(3)写出B与溴的四氯化碳溶液反应的化学方程式:________。
【答案】C4H8 C2H4 A 1-丁烯;顺-2-丁烯;反-2-丁烯;2-甲基丙烯 CH2=CH2+Br2 → BrCH2CH2Br
【解析】
(1)根据烃A分子中碳的质量分数,计算分子中C原子、H原子数目,写出A的分子式;由于A、B的最简式相同,再结合烃B式量比空气的平均式量稍小,推断B的分子式;
(2)烃A、B都能使溴的四氯化碳溶液褪色,含有不饱和键,根据A、B的分子式与结构判断是否存在同分异构体,根据结构及分子式书写限制条件的同分异构体;
(3)实验室制备乙烯是利用乙醇在浓硫酸催化作用发生消去反应生成。
(1)由于碳元素的质量分数为85.7%,所以烃A中C原子的数目为![]() =4,所以烃A中H原子的数目为
=4,所以烃A中H原子的数目为![]() =8,所以烃A的分子式为C4H8;A、B的最简式相同,最简式为CH2,B式量比空气的平均式量稍小,最简式CH2,所以B的分子式为C2H4;
=8,所以烃A的分子式为C4H8;A、B的最简式相同,最简式为CH2,B式量比空气的平均式量稍小,最简式CH2,所以B的分子式为C2H4;
(2)A为C4H8,B为C2H4,二者都能使溴的四氯化碳溶液褪色,说明分子中含有1个C=C双键,属于烯烃;A存在同分异构体,是CH2=CHCH2CH3,其名称是1-丁烯;CH3CH=CHCH3,存在顺反异构,其中: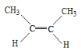 为顺-2-丁烯;
为顺-2-丁烯;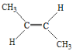 为反-2-丁烯;CH2=C(CH3)2为2-甲基丙烯;B不存在同分异构体。
为反-2-丁烯;CH2=C(CH3)2为2-甲基丙烯;B不存在同分异构体。

【题目】下表是元素周期表的一部分,表中的字母分别代表一种化学元素。
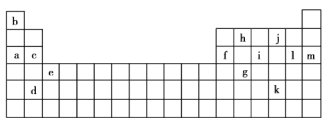
(1)a和c的I1大小关系是______大于______。(填字母)
(2)上述元素中,原子中未成对电子数最多的是______(填字母),写出该元素基态原子的核外电子排布式:______。
(3)根据下表所提供的电离能数据,回答下列问题。
锂 | X | Y | |
I1 | 520 | 496 | 580 |
I2 | 7296 | 4570 | 1820 |
I3 | 11799 | 6920 | 2750 |
I4 | 9550 | 11600 |
①表中X可能为以上13种元素中的______(填字母)元素。用元素符号表示![]() 和j形成的一种化合物的化学式:______。
和j形成的一种化合物的化学式:______。
②Y是周期表中第______族元素。
③以上13种元素中,______(填字母)元素原子失去核外第一个电子需要的能量最多。