题目内容
3.下列解释实验事实的离子方程式正确的是( )| A. | 用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-═Ag++NO↑+H2O | |
| B. | 漂白粉溶液中通入过量的SO2:ClO-+SO2+H2O═HClO+HSO3- | |
| C. | 酸性KI淀粉溶液久置后变蓝:4I-+O2+4H+═2I2+2H2O | |
| D. | Na2S溶液使酚酞试液变红:S2-+2H2O?2OH-+H2S |
分析 A.根据电子守恒判断,该反应中得失电子不相等;
B.次氯酸具有强氧化性,能够氧化亚硫酸氢根离子;
C.碘离子被空气中氧气氧化成碘单质;
D.硫离子的水解过程分步进行,水解的离子方程式需要分步写,且主要以第一步为主.
解答 解:A.用稀硝酸洗涤试管内壁的银镜,氧化还原反应必须满足电子式,正确的离子方程式为:3Ag+4H++NO3-═3Ag++NO↑+2H2O,故A错误;
B.漂白粉溶液中通入过量的SO2,反应生成硫酸钙沉淀、硫酸氯化氢,正确的离子方程式为:Ca2++2ClO-+2H2O+2SO2═CaSO4↓+SO42-+4H++2Cl-,故B错误;
C.酸性KI淀粉溶液久置后变蓝,碘离子被氧化成碘单质,反应的离子方程式为:4I-+O2+4H+═2I2+2H2O,故C正确;
D.硫化钠溶液中,硫离子部分水解生成硫氢化钠和氢氧根离子,溶液显示碱性,使酚酞试液变红,正确的离子方程式为:S2-+H2O?OH-+HS-,故D错误;
故选C.
点评 本题考查了离子方程式的书写判断,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案 期末好成绩系列答案
期末好成绩系列答案
相关题目
14.下列反应不属于可逆反应的是( )
| A. | 工业上利用氮气和氢气合成氨气 | |
| B. | 水电解生成氢氧混和气体和氢氧混和气体爆炸生成水 | |
| C. | 密闭容器中的二氧化氮和四氧化二氮在一定压力下可以相互转化 | |
| D. | 密闭容器中的二氧化硫和氧气在一定的条件下可以生成三氧化硫,同时三氧化硫又可以分解为二氧化硫和氧气 |
18.在800℃下测定反应2NO+2H2═N2+2H2O的反应物初始浓度及反应的初速率,所得数据如表所示
下列分析实验数据所得的结论中不正确的是( )
| 实验标号 | 初始浓度/mol•L-1 | 生成N2的初速率/mol•L-1•s-1 | |
| c(NO) | c(H2) | ||
| 1 | 6.00×10-3 | 1.00×10-3 | 3.19×10-3 |
| 2 | 6.00×10-3 | 2.00×10-3 | 6.38×10-3 |
| 3 | 6.00×10-3 | 3.00×10-3 | 9.57×10-3 |
| 4 | 1.00×10-3 | 6.00×10-3 | 0.48×10-3 |
| 5 | 2.00×10-3 | 6.00×10-3 | 1.92×10-3 |
| 6 | 3.00×10-3 | 6.00×10-3 | 4.32×10-3 |
| A. | 增大c(H2),生成N2的初速率增大 | B. | 减小c(NO),生成N2的初速率减小 | ||
| C. | 生成N2的初速率与c(H2)成正比 | D. | 生成N2的初速率与c(NO)成正比 |
8.下列关于乙醇的说法不正确的是( )
| A. | 可用淀粉的水解产物制取 | B. | 可由乙烯通过消去反应制取 | ||
| C. | 与甲醚(CH3OCH3)互为同分异构体 | D. | 通过氧化反应可制取乙醛 |
12.下列做法中,不利于环境保护的是( )
| A. | 燃煤脱硫,防止酸雨 | |
| B. | 使用无磷洗衣粉,防止水体污染 | |
| C. | 提倡使用含铅汽油,提高汽油的抗爆性 | |
| D. | 为燃料提供适当过量的空气,使燃料充分燃烧 |
 已知A、B、C、D、E都是元素周期表中前36号元素,它们的原子序数依次增大.A原子基态时最外层电子数是其内层电子总数的2倍,B原子基态时s电子数与p电子数相等,C在元素周期表的各元素中电负性最大,D原子基态时最外层成对电子对数是单电子数的3倍,E原子基态时未成对电子数是同周期元素中最多的.
已知A、B、C、D、E都是元素周期表中前36号元素,它们的原子序数依次增大.A原子基态时最外层电子数是其内层电子总数的2倍,B原子基态时s电子数与p电子数相等,C在元素周期表的各元素中电负性最大,D原子基态时最外层成对电子对数是单电子数的3倍,E原子基态时未成对电子数是同周期元素中最多的. ,1mol A22-中含有的π键数目为2NA
,1mol A22-中含有的π键数目为2NA ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧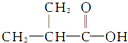 ⑨CH3CHBrCH3 ⑩
⑨CH3CHBrCH3 ⑩ ⑪
⑪
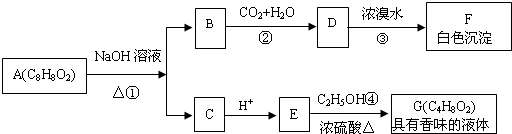
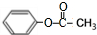 .
.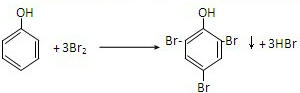 ,该反应的反应类型是取代反应.
,该反应的反应类型是取代反应. CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O. .
. .
.